题目内容
设NA为阿伏加德罗常数,下列叙述正确的是( )
| A、27g铝的原子最外层电子总数为NA |
| B、2.8 g N2和2.8 g CO所含电子数均为1.4NA |
| C、1L0.1mol?L-1乙酸溶液中H+数为0.1NA |
| D、标准状况下,22.4L乙醇的分子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.铝原子最外层含有3个电子,1mol铝原子最外层含有3mol电子;
B.氮气和一氧化碳的摩尔质量都是28g/mol,二者分子中都含有14个电子,2.8g氮气和一氧化碳的物质的量都是0.1mol,含有1.4mol电子;
C.乙酸为弱酸,溶液中只能部分电离出氢离子;
D.标准状况下,乙醇的状态不是气体,不能使用气体摩尔体积计算其物质的量.
B.氮气和一氧化碳的摩尔质量都是28g/mol,二者分子中都含有14个电子,2.8g氮气和一氧化碳的物质的量都是0.1mol,含有1.4mol电子;
C.乙酸为弱酸,溶液中只能部分电离出氢离子;
D.标准状况下,乙醇的状态不是气体,不能使用气体摩尔体积计算其物质的量.
解答:
解:A.27g铝的物质的量为1mol,1mol铝原子含有的最外层电子为3mol,含有的最外层电子总数为3NA,故A错误;
B.2.8g氮气的物质的量为0.1mol,含有1.4mol电子;2.8gCO的物质的量为0.1mol,含有1.4mol电子,二者所含电子数均为1.4NA,故B正确;
C.1L 0.1mol?L-1乙酸溶液中含有溶质乙酸0.1mol,由于乙酸只能部分电离出氢离子,则氢离子的物质的量一定小于0.1mol,溶液中含有的H+数小于0.1NA,故C错误;
D.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算22.4L乙醇的物质的量,故D错误;
故选B.
B.2.8g氮气的物质的量为0.1mol,含有1.4mol电子;2.8gCO的物质的量为0.1mol,含有1.4mol电子,二者所含电子数均为1.4NA,故B正确;
C.1L 0.1mol?L-1乙酸溶液中含有溶质乙酸0.1mol,由于乙酸只能部分电离出氢离子,则氢离子的物质的量一定小于0.1mol,溶液中含有的H+数小于0.1NA,故C错误;
D.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算22.4L乙醇的物质的量,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确分子、原子、原子核内质子中子及核外电子的构成关系,选项D为易错点,注意标况下乙醇、水、三氧化硫、氟化氢等的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量或体积.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列叙述正确的是( )
| A、测定相同温度下盐酸和醋酸溶液的pH,可证明盐酸是强酸、醋酸是弱酸 |
| B、改变温度能改变任何可逆反应的平衡状态 |
| C、离子反应的结果是自由移动的离子浓度减小 |
| D、Fe(OH)3胶体和饱和FeCl3溶液都呈红褐色,可通过丁达尔效应区分二者 |
2012年,将在京津冀、长三角、珠三角等重点区域以及直辖市和省会城市开展PM2.5(PM2.5是指大气中直径接近于2.5×10 -6m的颗粒物)和臭氧监测,下列有关说法正确的是( )
| A、PM2.5在空气中形成了气溶胶 |
| B、同温同压条件下,等质量的氧气和臭氧体积比为2:3 |
| C、16g臭氧中含有NA个原子 |
| D、1.00 mol臭氧中含有电子总数为18NA |
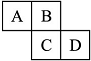 如图是元素周期表的一部分.A、B、C、D均为短周期元素,若C原子最外层电子数是其内层电子数的
如图是元素周期表的一部分.A、B、C、D均为短周期元素,若C原子最外层电子数是其内层电子数的| 3 |
| 5 |
| A、气态氢化物的稳定性:A>B |
| B、B元素的两种同素异形体常温下都是气体 |
| C、最高价氧化物对应水化物的酸性:D>C |
| D、原子半径从大到小的排列顺序为:C>B |
若NA表示阿伏加德罗常数的值.下列说法中正确的是( )
| A、500mL 2mol?L-1 葡萄糖溶液中所含分子数为NA |
| B、0.1mol?L-1Na2CO3溶液中的阴离子总数大于0.1NA |
| C、电解精炼铜时,若阳极质量减少64g,则外电路导线上不一定通过2 NA个电子 |
| D、标准状况下,22.4L NO和11.2L O2混合后气体的分子总数为1.5NA |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA |
| B、1 L 0.1 mol.L-1的醋酸溶液中氢离子数为0.1 NA |
| C、以惰性电极电解NaCl溶液时,每放出11.2LCl2时,则消耗NaCl个数为NA |
| D、在密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移的电子数为0.6NA |
设NA表示阿伏加德罗常数的值.下列有关说法正确的是( )
| A、在标准状况下,2.24L氮气含有共用电子对数的0.5NA |
| B、22.4g铁粉完全溶于一定浓度的硝酸中,转移的电子数可能为0.6NA |
| C、4.6g甲醇和二甲醚(CH3-O-CH3)的混合物中所含分子数等于0.1NA |
| D、含Al3+数目为0.1NA的硝酸铝溶液中,NO3-个数大于0.3NA |
同质量的下列气体中,所含原子数最少的是( )
| A、CH4 |
| B、CO2 |
| C、HCl |
| D、N2 |