题目内容
9.有X、Y、Z、W四种金属,已知:①X(OH)3的碱性强于Y(OH)2;②X3+可将Z氧化;③W可与热水反应产生H2,X不能与热水反应;④把X的金属片插入稀H2SO4中,让金属片与Z接触,则X溶解速率加快.下列四种金属活动性强弱关系中一定正确的是( )| A. | X>Y | B. | W>Z | C. | Z>Y | D. | Z>X |
分析 ①金属的活泼性强,最高价氧化物对应水化物的碱性就强;②X3+可将Z氧化,可以得到X3+的氧化性较强;③W可与热水反应产生H2,X不能与热水反应,说明金属活泼性是W大于X;④把X的金属片插入稀H2SO4中,让金属片与Z接触,则X溶解速率加快,此时X是原电池的负极,Z是正极.
解答 解:①金属的活泼性强,最高价氧化物对应水化物的碱性就强,但是不知道该碱是不是金属的最高价氧化物对应的水化物,所以金属活动性无法确定;②X3+可将Z氧化,可以得到X3+的氧化性较强;③W可与热水反应产生H2,X不能与热水反应,说明金属活泼性是W大于X;④把X的金属片插入稀H2SO4中,让金属片与Z接触,则X溶解速率加快,此时X是原电池的负极,Z是正极,所以金属的活泼性是X大于Z,根据③④得到金属活动性强弱关系:W>X>Z.
故选B.
点评 本题考查了金属活动性强弱顺序的判断,根据金属与水的置换反应、金属之间的置换反应确定金属性强弱,还可以根据金属的最高价氧化物的水化物碱性强弱判断,题目难度不大.

练习册系列答案
相关题目
20.检验溴乙烷中是否有溴元素,合理的实验方法是( )
| A. | 加入氯水后振荡,看水层里是否有棕红色的溴出现 | |
| B. | 加入硝酸银溶液,再加稀硝酸,观察有无浅黄色沉淀生成 | |
| C. | 加入NaOH水溶液共热,冷却后加硝酸银溶液,观察有无浅黄色沉淀生成 | |
| D. | 加入NaOH水溶液共热,冷却后用过量稀硝酸中和过量碱后,再加硝酸银溶液,观察有无浅黄色沉淀生成 |
17.下列有关物质的制备或保存方法正确的是( )
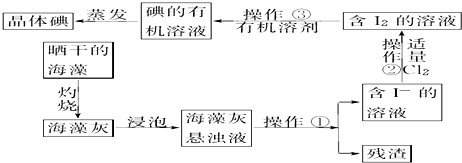
| A. | 实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 | |
| B. | 氢氧化钠溶液保存在玻璃塞的试剂瓶中 | |
| C. | 向氯化铝溶液滴入过量的氨水制备氢氧化铝 | |
| D. | 溴化银保存在无色玻璃瓶中 |
14.下列说法不正确的是( )
| A. | Na2O2用作呼吸面具的供氧剂 | B. | NaHCO3的热稳定性大于Na2CO3 | ||
| C. | 水可与金属钠反应放出氢气 | D. | 金属钠保存在煤油中 |
18.以下说法中正确的是( )
| A. | △S为负值的反应均不能自发进行 | |
| B. | △H<0的反应均是自发反应 | |
| C. | 高锰酸钾加热分解是一个熵减小的过程 | |
| D. | 冰在室温下自动熔化成水,是熵增的重要结果 |
19.下列实验的现象与对应结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| A. | A | B. | B | C. | C | D. | D |
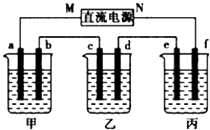 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g500%的NaOH溶液、足量的CuSO4溶液和l00g10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g500%的NaOH溶液、足量的CuSO4溶液和l00g10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题: (1)写出明矾[KAl(SO4)2•12H2O]在水中的电离方程式KAl(SO4)2•12H2O=K++Al3++2SO42-+12H2O,明矾净水的原因是因为它与水反应产生的Al(OH)3胶体具有吸附性.
(1)写出明矾[KAl(SO4)2•12H2O]在水中的电离方程式KAl(SO4)2•12H2O=K++Al3++2SO42-+12H2O,明矾净水的原因是因为它与水反应产生的Al(OH)3胶体具有吸附性.