题目内容
14.将2.1g CO和3.6g H2的混合气体与32g O2充分燃烧,立即通入足量的Na2O2固体中,则固体的质量增重( )| A. | 2.1g | B. | 3.6g | C. | 5.7g | D. | 37.7g |
分析 利用差量法,根据化学方程式分析:CO与H2在氧气中完全燃烧,生成CO2和H2O,生成的CO2和H2O再与Na2O2反应;2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应:2CO2+2Na2O2═2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应:2H2O+2Na2O2═4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量,据此进行分析.
解答 解:CO与H2在氧气中完全燃烧,生成CO2和H2O,CO2和H2O再与Na2O2反应,
反应2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2中一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应:2CO2+2Na2O2═2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;
反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O中生成的水与氢气物质的量相等,Na2O2与H2O反应:2H2O+2Na2O2═4NaOH+O2,质量增重△m=2H2O-O2=2H2,可知反应后固体增加的质量为氢气质量,
所以过氧化钠固体增重等于CO和H2的质量之和=2.1g+3.6g=5.7g,
故选C.
点评 本题考查混合物反应的计算,题目难度中等,注意从CO2、H2O与Na2O2生成固体质量的变化规律为解答该题的关键,试题培养了学生的分析、理解能力及灵活应用能力.

| A. | 8.96L | B. | 6.72L | C. | 5.6L | D. | 4.48L |
| A. | 铝热反应放出太量的热,因此可以用于冶炼高熔点金属 | |
| B. | 二氧化硅是一种熔沸点很高、硬度很大的氧化物 | |
| C. | 金刚石和石墨的化学性质相似,它们互为同素异形体 | |
| D. | 银白色的镁条在空气中剧烈燃烧后得到淡黄色固体 |
| A. | 汽油失火时,立即用水灭火 | |
| B. | 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 | |
| C. | 浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 | |
| D. | 实验室不小心碰翻酒精灯引起实验桌上洒落的少量酒精起火时,迅速用泡沫灭火器灭火 |
| A. | 乙醇的分子式C2H5OH | B. | 硫离子的结构示意图: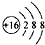 | ||
| C. | NH4Cl的电子式: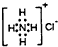 | D. | 对氯甲苯的结构简式: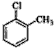 |