题目内容
2.配制2mol/L NaOH溶液2L,其中含有NaOH的物质的量为多少?需要称量NaOH多少克?分析 根据n=CV计算氢氧化钠物质的量,根据m=nM计算氢氧化钠质量,据此分析解答.
解答 解:n(NaOH)=2mol/L×2L=4mol,m(NaOH)=4mol×40g/mol=160g,
答:氢氧化钠的物质的量为4mol,其质量为160g.
点评 本题考查物质的量的有关计算,为高频考点,明确n、C、V、m、M之间的关系是解本题关键,题目难度不大.

练习册系列答案
相关题目
17.下列说法不正确的是( )
| A. | 浓硝酸保存在带有玻璃塞的棕色试剂瓶中 | |
| B. | 已经完成定容的500mL 1.0mol•L-1的NaOH溶液,某同学不慎将容量瓶中溶液洒出部分,继续加水至溶液凹液面与刻线相切 | |
| C. | 用托盘天平称量出12.50g的NaCl固体 | |
| D. | 物质溶于水的过程中,一般有放热或吸热现象,因此溶解的操作不能在量筒中进行 |
14.将2.1g CO和3.6g H2的混合气体与32g O2充分燃烧,立即通入足量的Na2O2固体中,则固体的质量增重( )
| A. | 2.1g | B. | 3.6g | C. | 5.7g | D. | 37.7g |
11.下列每步转化不能都通过一步实现的是( )
| A. | NH3→NO→NO2→HNO3 | B. | Al→Al2O3→Al(OH)3→NaAlO2 | ||
| C. | S→SO2→H2SO4→MgSO4 | D. | Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
1.下列各组物质中属于同分异构体的是( )
| A. | H2O和D2O | B. | 14C和12C | C. |  和 和 | D. |  和 和 |
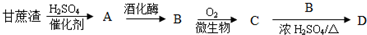

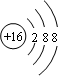 ,32g甲在足量浓硝酸中反应转移的电子数为2NA.
,32g甲在足量浓硝酸中反应转移的电子数为2NA.