题目内容
9.已知X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )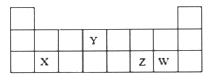
| A. | 原子半径:W>X | |
| B. | 氢化物的热稳定性:Z>W | |
| C. | 元素Y与元素Z可形成化合物YZ2 | |
| D. | 由氢化物水溶液的酸性:W>Z可推知元素的非金属性W>Z |
分析 X、Y、Z、W均为短周期元素,由元素在周期表的位置可知,X为Mg,Y为C,Z为S,W为Cl,
A.同周期从左向右原子半径减小;
B.同周期从左向右非金属性减弱,且非金属性越强,对应氢化物越稳定;
C.Y与Z形成的化合物与二氧化碳相似;
D.不能利用氢化物的酸性比较非金属性.
解答 解:X、Y、Z、W均为短周期元素,由元素在周期表的位置可知,X为Mg,Y为C,Z为S,W为Cl,
A.同周期从左向右原子半径减小,则原子半径:W<X,故A错误;
B.同周期从左向右非金属性减弱,且非金属性越强,对应氢化物越稳定,则氢化物的热稳定性:Z<W,故B错误;
C.Y与Z形成的化合物与二氧化碳相似,则元素Y与元素Z可形成化合物CS2,故C正确;
D.不能利用氢化物的酸性比较非金属性,比较非金属性的角度不合理,故D错误;
故选C.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,选项D为易错点,题目难度不大.

练习册系列答案
相关题目
5.已知氢化钠(NaH)是一种离子化合物,其中钠是+1价,NaH与水反应放出H2(NaH+H2O→NaOH+H2).下列叙述中正确的是( )
| A. | NaH在水中显酸性 | |
| B. | NaH中氢离子的电子层排布与氦原子相同 | |
| C. | NaH在反应中表现氧化性 | |
| D. | NaH中氢离子可被氧化成氢气 |
17.下列反应属于取代反应的是( )
| A. | 乙酸乙酯在酸性条件下水解 | B. | 乙炔使溴的四氯化碳溶液褪色 | ||
| C. | 由乙醇制乙烯 | D. | 甲苯使酸性KMnO4溶液褪色 |
4.下列属于电解质的是( )
| A. | 酒精 | B. | 石灰水 | C. | 碳酸钠 | D. | 铁 |
1.下列说法不正确的是( )
| A. | 一水合氨的电离方程式:NH3•H2O?NH4++OH- | |
| B. | 氯化镁的摩尔质量:95g | |
| C. | 亚硫酸的化学式:H2SO3 | |
| D. | Na+的结构示意图: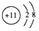 |
18.在一容积可变的密闭容器中,存在2HI(g)?H2(g)+I2(g)△H>0.欲使体系颜色加深,可采取的措施是( )
| A. | 缩小容器的体积 | B. | 在体积不变的情况下充入适量H2 | ||
| C. | 适当降低温度 | D. | 在保持压强不变情况下充入适量N2 |
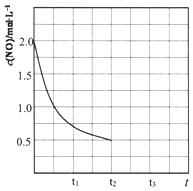 环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种.
环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种.