题目内容
1.下列说法不正确的是( )| A. | 一水合氨的电离方程式:NH3•H2O?NH4++OH- | |
| B. | 氯化镁的摩尔质量:95g | |
| C. | 亚硫酸的化学式:H2SO3 | |
| D. | Na+的结构示意图: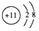 |
分析 A.一水合氨为弱电解质,部分电离,用可逆号;
B.摩尔质量以g/mol为单位,数值上等于其相对分子质量;
C.亚硫酸为二氧化硫对应的含氧酸,由H、S、O元素组成,分子中原子个数比为2:1:3;
D.结构示意图书写:圆内数字为原子的质子数,符号表示电性,圆外的弧线为电子层,弧线上的数字为该层上的电子数,离圆最近的弧线表示第一层,依次向外为第二层等,Na+的质子数为11,核外为10个电子.
解答 解:A.一水合氨为弱电解质,部分电离出铵根离子和氢氧根离子,电离方程式;NH3•H2O?NH4++OH-,故A正确;
B.氯化镁的相对分子质量为24+35.5×2=95,氯化镁的摩尔质量是95g/mol,故B错误;
C.亚硫酸为二氧化硫对应的含氧酸,由H、S、O元素组成,分子中原子个数比为2:1:3,分子式为H2SO3,故C正确;
D.Na+的质子数为11,有2个电子层,第一电子层容纳2个电子,第二电子层容纳8个电子,结构示意图为: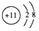 ,故D正确;
,故D正确;
故选B.
点评 本题考查化学用语的使用,为高频考点,把握电离方程式书写、物质的构成、结构示意图为解答的关键,侧重分析与应用能力的考查,注意化学用语的使用规范,题目难度不大.

练习册系列答案
相关题目
11.下列物质不能使橙色溴水变为无色溶液的是( )
| A. | CCl4多次萃取 | B. | 镁粉 | C. | Ba(OH)2溶液 | D. | KI溶液 |
12.某200mL Fe2(SO4)3溶液中含有0.1molFe3+,该溶液中SO42-的物质的量浓度为( )
| A. | 0.75mol/L | B. | 0.5mol/L | C. | 1mol/L | D. | 0.25mol/L |
9.已知X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )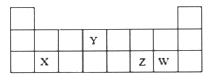

| A. | 原子半径:W>X | |
| B. | 氢化物的热稳定性:Z>W | |
| C. | 元素Y与元素Z可形成化合物YZ2 | |
| D. | 由氢化物水溶液的酸性:W>Z可推知元素的非金属性W>Z |
16.下列仪器名称为“分液漏斗”的是( )
| A. |  | B. |  | C. |  | D. |  |
6.下列说法正确的是( )
| A. | 焦炭炼铁、发酵粉烘焙糕点均会产生温室气体 | |
| B. | 浓硫酸滴在白纸上,白纸变黑,体现了浓硫酸的吸水性 | |
| C. | Cu与H2SO4在加热条件下发生反应,体现了浓H2SO4的还原性 | |
| D. | 雨水样品在空气中放置2小时后,测得pH变小,因为样品吸收了空气中的CO2 |
13.下列生活中常见物质的俗名与化学式相对应的是( )
| A. | 生石灰-Ca(OH)2 | B. | 重晶石-BaCO3 | C. | 明矾-CuSO4•5H2O | D. | 小苏打-NaHCO3 |
10.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 无色透明的溶液中:K+、Cu2+、NO3-、Cl- | |
| B. | 0.1 mol•L-1CaCl2溶液中:Mg2+、NH4+、CO32-、SO42- | |
| C. | pH=12的溶液:Na+、K+、SiO32-、Cl- | |
| D. | 使甲基橙变红的溶液中:Na+、Fe2+、NO3-、Cl- |
11.常温下,下列溶液中,酸性最强的是( )
| A. | pH=2的溶液 | B. | c(OH)=1×10-13mol/L | ||
| C. | c(H+)=1×10-5mol/L | D. | c(H2SO4)=0.75mol/L |