题目内容
5.已知氢化钠(NaH)是一种离子化合物,其中钠是+1价,NaH与水反应放出H2(NaH+H2O→NaOH+H2).下列叙述中正确的是( )| A. | NaH在水中显酸性 | |
| B. | NaH中氢离子的电子层排布与氦原子相同 | |
| C. | NaH在反应中表现氧化性 | |
| D. | NaH中氢离子可被氧化成氢气 |
分析 氢化钠中含有钠离子和氢离子,为离子晶体,氢化钠和水反应生成氢气,反应方程式为:NaH+H2O=NaOH+H2↑,该反应中氢元素化合价由-1价、+1价变为0价,据此分析解答.
解答 解:A.氢化钠和水反应生成氢氧化钠,氢氧化钠是强碱,所以其溶液呈碱性,故A错误;
B.NaH中H元素是-1价,其核外电子数为2,所以其电子层排布与氦原子的相同,故B正确;
C.氢化钠中氢元素的化合价由-1价变为0价,表现还原性,故C错误;
D.氢化钠中氢元素的化合价由-1价变为0价,氢离子失电子被氧化生成氢气,故D正确;
故选BD.
点评 本题考查了氢化钠的有关知识,明确氢化钠中氢离子的结构是解本题关键,注意氢化钠中氢元素显-1价,为易错点.

练习册系列答案
相关题目
15.下列物质能使品红溶液褪色,且褪色原理基本相同的是( )
①活性炭 ②氯水 ③二氧化硫 ④臭氧 ⑤过氧化钠.
①活性炭 ②氯水 ③二氧化硫 ④臭氧 ⑤过氧化钠.
| A. | ①②④⑥ | B. | ①②③⑤ | C. | ②④⑤ | D. | ③④⑤ |
16.高温下FeSO4发生反应:2FeSO4→Fe2O3+SO2↑+SO3↑,若将生成的气体通入足量的BaCl2溶液中,则( )
| A. | 只产生BaSO4沉淀 | B. | 只产生BaSO3沉淀 | ||
| C. | 一定有BaSO4和BaSO3沉淀 | D. | 一定有SO2、SO3气体逸出 |
13.氢硫酸溶液与下列少量物质反应后,能使溶液酸性增强的是( )
①O2②I2③Pb(Ac)2④CuSO4.
①O2②I2③Pb(Ac)2④CuSO4.
| A. | ①③ | B. | ②④ | C. | ②③④ | D. | ① |
20.下列物质保存方法正确的是( )
| A. | 氯水保存在无色试剂瓶中 | |
| B. | 氢氟酸(HF)保存在玻璃试剂瓶中 | |
| C. | 过氧化钠(Na2O2)密闭保存且远离可燃物 | |
| D. | 金属钠保存在CCl4中 |
4.三乙醇铝(AlC6H15O3)是酯化反应及聚合反应的催化剂,遇水分解生成氢氧化铝,可由无水乙醇与铝汞合金反应制备,下列有关叙述或表示正确的是( )
| A. | 乙醇的结构式为C2H6O | |
| B. | 中子数为14的铝原子可表示为${\;}_{13}^{14}$Al | |
| C. | 铝汞合金的熔点比金属铝的高 | |
| D. | Al(OH)3的电离方程式为H++AlO2-+H2O?Al(OH)3?Al3++3OH- |
11.下列物质不能使橙色溴水变为无色溶液的是( )
| A. | CCl4多次萃取 | B. | 镁粉 | C. | Ba(OH)2溶液 | D. | KI溶液 |
8.“足球烯”C60是一种外形类似足球状的分子,关于C60的说法错误的是( )
| A. | C60是一种新型的化合物 | B. | C60是相对分子量为720 | ||
| C. | C60和金刚石互为同素异形体 | D. | C60硬度比金刚石小 |
9.已知X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )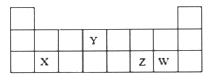

| A. | 原子半径:W>X | |
| B. | 氢化物的热稳定性:Z>W | |
| C. | 元素Y与元素Z可形成化合物YZ2 | |
| D. | 由氢化物水溶液的酸性:W>Z可推知元素的非金属性W>Z |