题目内容
(I)羧酸与醇发生酯化反应,通常有不稳定的中间产物生成.例如:
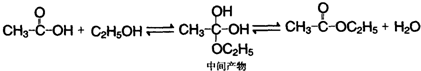
现以环己烯(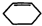 )为原料,通过以下各步转化,最终可制得有机物
)为原料,通过以下各步转化,最终可制得有机物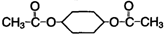 (部分反应过程及反应条件略去)
(部分反应过程及反应条件略去)
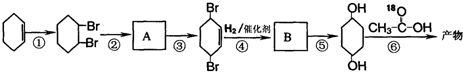
请回答下列问题:
(1)写出结构简式:A ;B .
(2)第⑥步反应生成的酯和水中都含有18O,请简述理由 .
(II)已知:卤代烃可发生如下反应:
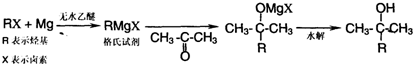
(3)请仿照上例设计一条由1-丙醇合成-2-甲基-1-丙醇的路线. .

现以环己烯(
 )为原料,通过以下各步转化,最终可制得有机物
)为原料,通过以下各步转化,最终可制得有机物 (部分反应过程及反应条件略去)
(部分反应过程及反应条件略去)
请回答下列问题:
(1)写出结构简式:A
(2)第⑥步反应生成的酯和水中都含有18O,请简述理由
(II)已知:卤代烃可发生如下反应:

(3)请仿照上例设计一条由1-丙醇合成-2-甲基-1-丙醇的路线.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:(I)(1)环己烯 与溴发生加成反应生成
与溴发生加成反应生成 ,由A的反应产物可知,
,由A的反应产物可知, 发生消去反应生成A为
发生消去反应生成A为 ,A与溴发生1,4-加成反应生成
,A与溴发生1,4-加成反应生成 ,
, 与氢气发生加成反应生成B为
与氢气发生加成反应生成B为 ,B在氢氧化钠水溶液、加热条件下发生水解反应生成
,B在氢氧化钠水溶液、加热条件下发生水解反应生成 ,再与乙酸发生转化反应生成
,再与乙酸发生转化反应生成 ,
,
(2)根据中间产物中羟基脱水方式可知,生成的酯和水中都含有18O;
(II)1-丙醇在浓硫酸、加热条件下发生消去反应生成CH3CH=CH2,再与HCl发生加成反应生成CH3CHClCH3,CH3CHClCH3无水乙醚、Mg条件下得到(CH3)2CHMgCl,(CH3)2CHMgCl与HCHO反应得到(CH3)2CHCH2OMgCl,(CH3)2CH2OMgCl再发生水解反应得到(CH3)2CHCH2OH.
 与溴发生加成反应生成
与溴发生加成反应生成 ,由A的反应产物可知,
,由A的反应产物可知, 发生消去反应生成A为
发生消去反应生成A为 ,A与溴发生1,4-加成反应生成
,A与溴发生1,4-加成反应生成 ,
, 与氢气发生加成反应生成B为
与氢气发生加成反应生成B为 ,B在氢氧化钠水溶液、加热条件下发生水解反应生成
,B在氢氧化钠水溶液、加热条件下发生水解反应生成 ,再与乙酸发生转化反应生成
,再与乙酸发生转化反应生成 ,
,(2)根据中间产物中羟基脱水方式可知,生成的酯和水中都含有18O;
(II)1-丙醇在浓硫酸、加热条件下发生消去反应生成CH3CH=CH2,再与HCl发生加成反应生成CH3CHClCH3,CH3CHClCH3无水乙醚、Mg条件下得到(CH3)2CHMgCl,(CH3)2CHMgCl与HCHO反应得到(CH3)2CHCH2OMgCl,(CH3)2CH2OMgCl再发生水解反应得到(CH3)2CHCH2OH.
解答:
解:(I)(1)环己烯 与溴发生加成反应生成
与溴发生加成反应生成 ,由A的反应产物可知,
,由A的反应产物可知, 发生消去反应生成A为
发生消去反应生成A为 ,A与溴发生1,4-加成反应生成
,A与溴发生1,4-加成反应生成 ,
, 与氢气发生加成反应生成B为
与氢气发生加成反应生成B为 ,B在氢氧化钠水溶液、加热条件下发生水解反应生成
,B在氢氧化钠水溶液、加热条件下发生水解反应生成 ,再与乙酸发生转化反应生成
,再与乙酸发生转化反应生成 ,故答案为:
,故答案为: ;
; ;
;
(2)因为中间产物有两种脱水方式: 和
和 ,故生成的酯和水中都含有18O,
,故生成的酯和水中都含有18O,
故答案为:中间产物有两种脱水方式: 和
和 ,故生成的酯和水中都含有18O;
,故生成的酯和水中都含有18O;
(II)(3)1-丙醇在浓硫酸、加热条件下发生消去反应生成CH3CH=CH2,再与HCl发生加成反应生成CH3CHClCH3,CH3CHClCH3无水乙醚、Mg条件下得到(CH3)2CHMgCl,(CH3)2CHMgCl与HCHO反应得到(CH3)2CHCH2OMgCl,(CH3)2CH2OMgCl再发生水解反应得到(CH3)2CHCH2OH,由1-丙醇合成-2-甲基-1-丙醇的路线流程图为: ,
,
故答案为: .
.
 与溴发生加成反应生成
与溴发生加成反应生成 ,由A的反应产物可知,
,由A的反应产物可知, 发生消去反应生成A为
发生消去反应生成A为 ,A与溴发生1,4-加成反应生成
,A与溴发生1,4-加成反应生成 ,
, 与氢气发生加成反应生成B为
与氢气发生加成反应生成B为 ,B在氢氧化钠水溶液、加热条件下发生水解反应生成
,B在氢氧化钠水溶液、加热条件下发生水解反应生成 ,再与乙酸发生转化反应生成
,再与乙酸发生转化反应生成 ,故答案为:
,故答案为: ;
; ;
;(2)因为中间产物有两种脱水方式:
 和
和 ,故生成的酯和水中都含有18O,
,故生成的酯和水中都含有18O,故答案为:中间产物有两种脱水方式:
 和
和 ,故生成的酯和水中都含有18O;
,故生成的酯和水中都含有18O;(II)(3)1-丙醇在浓硫酸、加热条件下发生消去反应生成CH3CH=CH2,再与HCl发生加成反应生成CH3CHClCH3,CH3CHClCH3无水乙醚、Mg条件下得到(CH3)2CHMgCl,(CH3)2CHMgCl与HCHO反应得到(CH3)2CHCH2OMgCl,(CH3)2CH2OMgCl再发生水解反应得到(CH3)2CHCH2OH,由1-丙醇合成-2-甲基-1-丙醇的路线流程图为:
 ,
,故答案为:
 .
.
点评:本题考查有机物推断与合成,注意根据转化关系中有机物结构进行推断,需要学生熟练掌握官能团的性质与转化,(II)中合成需要学生对给予的信息进行利用,较好的考查学生的自学能力与知识迁移应用,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在一种pH=1的溶液中可能存在NO3-,I-,Cl-,Fe3+中的一种或几种.向该溶液中滴入溴水,单质溴被还原.由此推断该溶液( )
| A、含NO3-,Fe3+,无I-,可能有Cl- |
| B、含I-,不含NO3-,Fe3+,可能有Cl- |
| C、含I-,Fe3+,不含NO3-,可能有Cl- |
| D、含NO3-,不含I-,Fe3+,可能有Cl- |
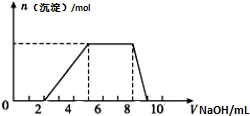 某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、AlO2-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、AlO2-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )| A、原溶液中一定含有的阳离子是H+、Mg2+、Al3+、NH4+ |
| B、反应最后形成的溶液中的溶质含AlCl3 |
| C、原溶液中Al3+与NH4+的物质的量之比1:3 |
| D、原溶液中含有的阴离子是AlO2-、Cl- |
下列装置可以达到相关实验目的是(部分夹持固定装置略去)( )
| A | B | C | D |
 |  |  |  |
| 将开关K置于M或N处以减缓铁的腐蚀 | 蒸干NH4Cl饱和溶液以制备NH4Cl晶体 | 证明Ag+的氧化性强于Cu2+ | 干燥、收集并吸收多余的NH3 |
| A、A | B、B | C、C | D、D |
石棉是一类价格低廉的硅酸盐材料,有毒、能使人患肺癌.一种青石棉的化学式为:Na2Fe5Si8O22(OH)2,它用足量稀硝酸溶液处理时,还原产物只有NO,下列说法正确的是( )
| A、该物质中铁元素的化合价为+2价 |
| B、该物质的化学式组成可表示为:Na20.3FeO.Fe2O3.8SiO2.H2O |
| C、1mol该物质能和18mol HNO3反应,也能与18mol HCl反应 |
| D、这种石棉属于新型无机非金属材料 |
 如图是制取、干燥和收集某气体的实验装置,可用于( )
如图是制取、干燥和收集某气体的实验装置,可用于( )| A、用Zn与稀H2SO4反应制H2 |
| B、用CaO与浓氨水反应制NH3 |
| C、用Cu与稀HNO3反应制NO |
| D、用MnO2与浓HCl反应制C12 |

 工业上测量SO2、N2、O2混合气体中SO2含量的装置如图.反应管中装有碘的淀粉溶液.SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O═H2SO4+2HI
工业上测量SO2、N2、O2混合气体中SO2含量的装置如图.反应管中装有碘的淀粉溶液.SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O═H2SO4+2HI
