题目内容
下列电离方程式中,不正确的是( )
| A、CH3COOH?CH3COO-+H+ |
| B、Fe2(SO4)3═2Fe2++3SO42- |
| C、Ba(OH)2═Ba2++2OH- |
| D、NaHCO3═Na++HCO3- |
| E、NaHCO3═Na++HCO3- |
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:A.乙酸为弱酸部分电离;
B.硫酸铁电离出三价铁离子和硫酸根离子;
C.氢氧化钡为二元强碱,一步完全电离;
D.碳酸为二元弱酸,碳酸氢根离子部分电离,碳酸氢钠为强电解质完全电离出钠离子和碳酸氢根离子.
B.硫酸铁电离出三价铁离子和硫酸根离子;
C.氢氧化钡为二元强碱,一步完全电离;
D.碳酸为二元弱酸,碳酸氢根离子部分电离,碳酸氢钠为强电解质完全电离出钠离子和碳酸氢根离子.
解答:
解:A.乙酸是弱电解质,在水溶液里部分电离,电离方程式为CH3COOH?CH3COO-+H+,故A正确;
B.硫酸铁为强电解质,在水溶液中或熔融状态下完全电离出铁离子和硫酸根离子Fe2(SO4)3═2Fe3++3SO42-,故B错误;
C.氢氧化钡为二元强碱,一步完全电离Ba(OH)2═Ba2++2OH-,故C正确;
D.碳酸为二元弱酸,碳酸氢根离子部分电离,碳酸氢钠为强电解质完全电离NaHCO3═Na++HCO3-,故D正确;
故选B.
B.硫酸铁为强电解质,在水溶液中或熔融状态下完全电离出铁离子和硫酸根离子Fe2(SO4)3═2Fe3++3SO42-,故B错误;
C.氢氧化钡为二元强碱,一步完全电离Ba(OH)2═Ba2++2OH-,故C正确;
D.碳酸为二元弱酸,碳酸氢根离子部分电离,碳酸氢钠为强电解质完全电离NaHCO3═Na++HCO3-,故D正确;
故选B.
点评:本题考查了电离方程式的书写,根据电解质强弱确定“=”“?”,书写电离方程式时注意离子的正确书写、电荷守恒、离子团不能拆开,题目难度不大.

练习册系列答案
相关题目
在主量子数为4的电子层中,能容纳的最多电子数是 ( )
| A、18 | B、24 | C、32 | D、36 |
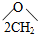
扑热息痛是一种优良的解热镇痛剂,其结构式为 ,对此不正确的说法是( )
,对此不正确的说法是( )
 ,对此不正确的说法是( )
,对此不正确的说法是( )| A、该物质水解后不能得到α-氨基酸 |
| B、该物质与苯丙氨酸互为同分异构体 |
| C、该物质能与浓溴水发生取代反应 |
D、该物质可由 和CH3COOH经缩合而成 和CH3COOH经缩合而成 |
下列反应中,属于取代反应的是( )
A、CH2═CH2+H2O
| |||
B、CH3CH2Br+NaOH
| |||
C、2CH3CHO+O2
| |||
D、2CH2═CH2+O2
 -CH2 -CH2 |
下列实验操作先后顺序正确的是( )
| A、先检查装置的气密性,后装好药品 |
| B、先用双手握紧试管,后将导管插入水中以检查装置的气密性 |
| C、用排水集气法集满气体后,先熄灭酒精灯,后撤导气管 |
| D、结束碳酸氢钠热稳定性的实验时,先撤导气管,后熄灭酒精灯 |
下列叙述正确的是( )
| A、钠和水反应放出氢气 |
| B、钠与硫的化合反应属于吸热反应 |
| C、钠在空气中燃烧生成Na2O |
| D、钠的密度比相同条件下的钾的密度小 |
23gNa与过量O2反应生成Na2O和Na2O2的混合物,O2得到电子( )
| A、1mol |
| B、2mol |
| C、4mol |
| D、2mol~4mol之间 |
下列实验方法及操作正确的是( )
| A、可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 |
| B、使用pH试纸测定未知气体的酸碱性时,不能用蒸馏水润湿试纸 |
| C、将20g KNO3完全溶于80 mL水中,配制质量分数约为20%的KNO3溶液 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应恰好相等 |