题目内容
4.A、B、C、D是四种有机物,它们的分子中含有相同的碳原子数,其中A和B是烃.在标准状况下,A对氢气的相对密度是13,B与HCl反应生成C,C与D混合后加入NaOH并加热,可生成B.(1)判断A、B、C、D各是哪种有机物,写出它们的结构简式A:CH≡CH、B:CH2═CH2、C:CH3CH2Cl、D:C2H5OH.
(2)写出相应的方程式.CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl、CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2═CH2+NaCl+H2O.
分析 A、B、C、D是四种有机物,它们的分子中含有相同的碳原子数,其中A和B是烃,在标准状况下,A对氢气的相对密度是13,则A的相对分子质量是26,结构简式为CH≡CH,B与HCl反应生成C,且B是烃,则B为CH2═CH2,C为CH3CH2Cl,CH3CH2Cl与D混合后加入NaOH并加热,可生成CH2═CH2,氯乙烷在氢氧化钠的醇溶液中发生消去反应生成乙烯,所以D为CH3CH2OH,据此分析解答.
解答 解:A、B、C、D是四种有机物,它们的分子中含有相同的碳原子数,其中A和B是烃,在标准状况下,A对氢气的相对密度是13,则A的相对分子质量是26,结构简式为CH≡CH,B与HCl反应生成C,且B是烃,则B为CH2═CH2,C为CH3CH2Cl,CH3CH2Cl与D混合后加入NaOH并加热,可生成CH2═CH2,氯乙烷在氢氧化钠的醇溶液中发生消去反应生成乙烯,所以D为CH3CH2OH,
(1)通过以上分析知,A、B、C、D为A:CH≡CH、B:CH2═CH2、C:CH3CH2Cl、D:C2H5OH,
故答案为:A:CH≡CH、B:CH2═CH2、C:CH3CH2Cl、D:C2H5OH;
(2)乙烯和HCl在一定条件下发生加成反应生成氯乙烷,反应方程式为CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl,
氯乙烷和NaOH的醇溶液在加热条件下发生消去反应生成乙烯,反应方程式为CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2═CH2+NaCl+H2O,
故答案为:CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl、CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2═CH2+NaCl+H2O.
点评 本题考查有机物推断,为高考高频点,涉及炔、烯烃、氯代烃之间的转化,明确常见物质的官能团及其性质是解本题关键,熟练掌握烷烃、烯烃、醇、卤代烃、醛、羧酸、酯之间的转化及反应条件,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 质子数 | B. | 中子数 | C. | 电子数 | D. | 质量数 |
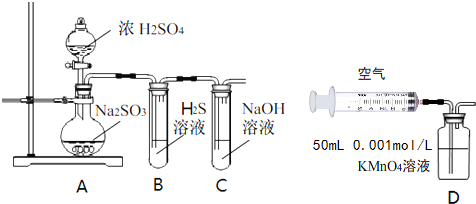
(1)写出A中的反应化学方程式Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O
(2)实验时,旋开装置A中分液漏斗的旋塞,发现液体流出缓慢,最终停止,其可能的原因是没有打开分液漏斗的上口活塞或分液漏斗上口活塞上的凹槽没有与分液漏斗上的小孔连通,导致无法与外界大气连通.
(3)装置B中的溶液出现浑浊,该实验证明SO2具有氧化性性.
(4)实验后,测定装置C中溶液呈碱性.溶液为什么呈碱性呢?大家有不同意见:①是生成的Na2SO3水解;②是氢氧化钠剩余.请设计实验方案证明哪种意见成立.选用下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
| 实验步骤 | 实验操作 | 预期现象与结论 |
| A. | A的相对分子质量比B的大16 | |
| B. | 该酯分子结构中一定存在双键 | |
| C. | B的相对分子质量比A大14 | |
| D. | 酯、A、B 3种分子中都含有一种相对分子质量大于60的相同基团 |
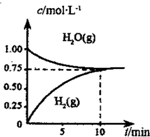 工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,在一定条件下,向体积为1L的密闭容器中充入1mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是( )
工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,在一定条件下,向体积为1L的密闭容器中充入1mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是( )| A. | 达平衡时,CH4(g)的转化率为75% | |
| B. | 0~10min内,v(CO)=0.075mol•L-1•min-1 | |
| C. | 该反应的化学平衡常数K=O.1875 | |
| D. | 当CH4(g)的消耗速率与H2(g)的消耗速率相等时,反应到达平衡 |
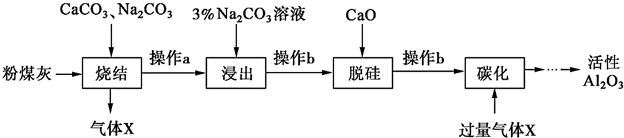
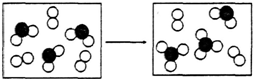 A、B、C、D、E、F是原子序数依次增大的短周期元素,B是短周期中金属性最强的元素,C是地壳中含量最高的金属元素,D单质的晶体是良好的半导体材料,E的最外层电子数与内层电子数之比为3:5,A与E同族.
A、B、C、D、E、F是原子序数依次增大的短周期元素,B是短周期中金属性最强的元素,C是地壳中含量最高的金属元素,D单质的晶体是良好的半导体材料,E的最外层电子数与内层电子数之比为3:5,A与E同族.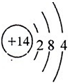
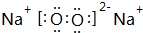 .
. Al(OH)3﹢3H+,生氢氧化铝胶体,能吸附水中悬浮物,使之凝聚达到净水目的
Al(OH)3﹢3H+,生氢氧化铝胶体,能吸附水中悬浮物,使之凝聚达到净水目的