题目内容
6.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 1molH2O含有的H2O分子数为NA | |
| B. | 1mol金属镁与足量的盐酸完全反应,转移的电子数为2NA | |
| C. | 11.2L氧气含有的O2分子数为0.5NA | |
| D. | 将含1molFeCl3的溶液与沸水完全反应,生成的Fe(OH)3胶体粒子数为NA |
分析 A、分子个数N=nNA;
B、镁与盐酸反应后变为+2价;
C、氧气所处的状态不明确;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体.
解答 解:A、分子个数N=nNA=1mol×NA/mol=NA个,故A正确;
B、镁与盐酸反应后变为+2价,故1mol镁反应转移2mol电子即2NA个,故B正确;
C、氧气所处的状态不明确,故氧气的物质的量和分子个数无法计算,故C错误;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故1mol氯化铁形成的胶粒的个数小于NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
16.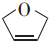 是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )
是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )
 是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )
是一种有机烯醚,具有旋光性和吸湿性.下列说法正确的是 ( )| A. | 分子式为C4H6O | B. | 能使溴水褪色 | C. | 能与钠发生反应 | D. | 能发生消去反应 |
17.核潜艇上的核反应堆内使用了液体铝合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
| A. | 离子半径:Na+>Al3+ | |
| B. | 铝钠合金若投入一定水中可得无色溶液并产生气泡 | |
| C. | 若mg不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越少 | |
| D. | 铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出 |
18.下列实验操作中正确的是( )
| A. | 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 | |
| B. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴单质 | |
| C. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| D. | 蒸馏操作时,应向蒸馏烧瓶中加入几块沸石,以防止暴沸 |
15.在实验室里,要想使氯化铝溶液中的铝离子全部沉下来,应选用( )
| A. | 石灰水 | B. | 氢氧化钠溶液 | C. | 硫酸 | D. | 氨水 |
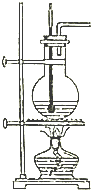 实验室用如图所示装置制取乙烯,请回答下列有关该实验的问题:
实验室用如图所示装置制取乙烯,请回答下列有关该实验的问题: