题目内容
纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”,Na2S2O3和Cl2反应的产物之一为H2SO4,写出该反应的离子方程式: .
考点:离子方程式的书写
专题:离子反应专题
分析:反应中Na2S2O3→H2SO4,S硫元素平均化合价由+2价升高为+6价,Na2S2O3是还原剂,Cl2→NaCl、HCl,Cl元素化合价由0价降低为-1价,Cl2是氧化剂,根据电子转移相等来配平即可.
解答:
解:反应中Na2S2O3→H2SO4,S硫元素平均化合价由+2价升高为+6价,Na2S2O3是还原剂,Cl2→NaCl、HCl,Cl元素化合价由0价降低为-1价,Cl2是氧化剂,根据电子转移相等,所以n(Na2S2O3)×2×(6-2)=n(Cl2)×2,故n(Na2S2O3):n(Cl2)=1:4,方程式为:5H2O+S2O32-+4Cl2=2SO42-+8Cl-+10H+,
故答案为:5H2O+S2O32-+4Cl2=2SO42-+8Cl-+10H+.
故答案为:5H2O+S2O32-+4Cl2=2SO42-+8Cl-+10H+.
点评:本题考查了离子方程式的书写、氧化还原反应的配平,题目难度中等,抓住反应物的性质特点,分析产物,写出反应的离子方程式,平时学习应注意理解记忆.

练习册系列答案
相关题目
下列用来表示物质变化的化学用语中,正确的是( )
| A、NH4NO3溶液呈酸性的原因:NH4++H2O=NH3?H2O+H+ |
| B、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| C、硫酸氢钠溶液中滴加少量Ba(OH)2溶液的离子方程式:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓ |
D、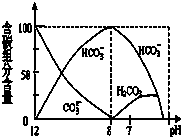 如图是在0.1 mol?L-1Na2CO3溶液中逐滴加入0.1 mol?L-1 HCl,则 pH=7时的离子方程式:H++HCO3-=CO2↑+H2O |
 某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入Fe粉,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如如图所示.则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入Fe粉,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如如图所示.则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )| A、1:1:1 |
| B、1:1:4 |
| C、1:2:2 |
| D、3:2:8 |
对于同位素的概念,下列叙述中正确的是( )
| A、原子序数相等,化学性质与质量数不同 |
| B、原子序数相等,并有相同的化学性质和相同的质量数 |
| C、原子序数相等,化学性质几乎完全相同,而中子数不同 |
| D、化学性质相同,而质量数与原子序数不同 |
某一有机物A(C8H16O2)可发生如图变化;已知B为羧酸,且D氧化可以得到B,则A的可能结构有( )
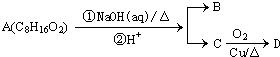
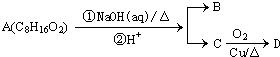
| A、1种 | B、2种 | C、3种 | D、4种 |
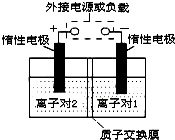 全钒液流储能电池,是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置.现将钒的相关化合物溶解在pH=1的稀硫酸中,按下图组装一个模拟电池.
全钒液流储能电池,是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置.现将钒的相关化合物溶解在pH=1的稀硫酸中,按下图组装一个模拟电池.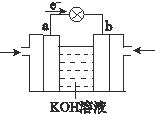 A、B、C、D、E为五种原子序数逐渐增大的短周期元素,其中 A与B组成的化合物是一种温室气体,B与D、C与D组成的化合物是机动车排出的大气污染物,D和E能形成原子个数比为1:1和1:2的两种离子化合物.
A、B、C、D、E为五种原子序数逐渐增大的短周期元素,其中 A与B组成的化合物是一种温室气体,B与D、C与D组成的化合物是机动车排出的大气污染物,D和E能形成原子个数比为1:1和1:2的两种离子化合物.