题目内容
9.下列实验操作或事实与预期实验目的或所得结论对应正确的是( )| A. | 淡黄色试液$\stackrel{NaOH溶液}{→}$红褐色沉淀 说明原溶液中一定含有FeCl3 | |
| B. | H3PO3+2NaOH(足量)=Na2HPO3+2H2O,H3PO3属于三元酸 | |
| C. | 新收集的酸雨$\stackrel{Ba(NO_{3})_{2}溶液}{→}$白色沉淀酸雨中一定含有SO42- | |
| D. | CaO$\stackrel{H_2{O}}{→}$Ca(OH)2$\stackrel{Na_{2}CO_{3}}{→}$NaOH 用生石灰制备NaOH溶液 |
分析 A.能和NaOH溶液产生红褐色沉淀的离子是Fe3+,原溶液中的溶质为可溶性铁盐;
B.NaOH足量,生成的Na2HPO3为正盐;
C.新收集的酸雨含亚硫酸,与硝酸钡发生氧化还原反应生成硫酸钡;
D.CaO与水反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙和NaOH.
解答 解:A.能和NaOH溶液产生红褐色沉淀的离子是Fe3+,原溶液中的溶质为可溶性铁盐,淡黄色试液$\stackrel{NaOH溶液}{→}$红褐色沉淀 说明原溶液中一定含Fe3+,但溶质不一定是FeCl3,故A错误;
B.NaOH足量,生成的Na2HPO3为正盐,则H3PO3属于二元酸,故B错误;
C.新收集的酸雨含亚硫酸,与硝酸钡发生氧化还原反应生成硫酸钡,不能说明是否含SO42-,故C错误;
D.CaO与水反应生成氢氧化钙,氢氧化钙与碳酸钠发生复分解反应生成碳酸钙和NaOH,则由实验操作可用生石灰制备NaOH溶液,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及离子检验、物质检验、物质制备等知识点,明确离子及物质性质是解本题关键,注意:离子检验时要排除其它离子干扰,题目难度不大.

练习册系列答案
相关题目
19.向甲溶液中缓慢滴加乙溶液,反应生成沉淀的质量与乙溶液的量之间的关系如图所示,其中符合图象的是( )
| 甲 | 乙 | 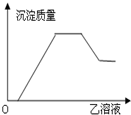 | |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH | |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 | |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH | |
| D | NaAlO2、氨水、NaOH | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
20.300℃时,将100mL由H2O、CO2和N2组成的混合气体通入盛有足量Na2O2的密闭容器中(容器体积保持不变),充分反应后恢复到原温度时容器内的压强变为原来的$\frac{4}{5}$.则原混合气体中N2的体积分数为( )
| A. | 33.3% | B. | 40% | C. | 60% | D. | 75% |
4.三氯化磷(PCl3)是一种重要的掺杂剂.实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示:(部分夹持装置略去)
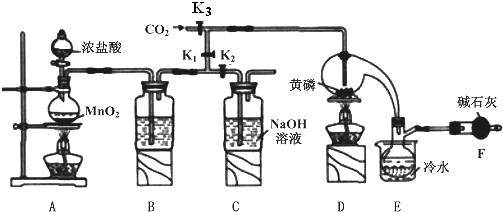
已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和气体;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
请回答下列问题:
(1)B中所装试剂是浓硫酸;
E中冷水的作用是冷凝PCl3防止其挥发.
(2)F中碱石灰的作用是吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3 反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O.
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL.
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为79.75%.

已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和气体;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)B中所装试剂是浓硫酸;
E中冷水的作用是冷凝PCl3防止其挥发.
(2)F中碱石灰的作用是吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3 反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O.
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL.
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为79.75%.
18.下列反应中的氨与反应4NH3+5O2→4NO+6H2O中的氨作用相同的是( )
| A. | 2NH3+3CuO→3Cu+N2+3H2O | B. | 2Na+2NH3→2NaNH2+H2↑ | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |