题目内容
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)?NH3(g)+HI(g)②2HI(g)?H2(g)+I2(g)
达到平衡时,c(H2)=0.5mol?L-1,c(NH3)=4mol?L-1,则此温度下反应①的平衡常数为( )
①NH4I(s)?NH3(g)+HI(g)②2HI(g)?H2(g)+I2(g)
达到平衡时,c(H2)=0.5mol?L-1,c(NH3)=4mol?L-1,则此温度下反应①的平衡常数为( )
| A、9 | B、12 | C、16 | D、20 |
考点:化学平衡的计算
专题:化学平衡专题
分析:反应①的平衡常数k=c(NH3)?c(HI),NH4I分解生成的HI为平衡时HI与分解的HI之和,即为NH4I分解生成的NH3,由反应②可知分解的c(HI)为平衡时c(H2)的2倍,求出为NH4I分解生成的NH3,代入反应①的平衡常数K=c(NH3)?c(HI)计算.
解答:
解:平衡时c(NH3)=4mol?L-1,NH4I分解生成的HI的浓度为4mol?L-1,HI分解生成的H2的浓度为0.5mol?L-1.最后平衡状态HI的浓度为4mol?L-1-2×0.5mol?L-1=3mol/L,所以反应①的平衡常数K=c(NH3)?c(HI)=4mol?L-1×3mol?L-1=12mol2?L-2.
故选B.
故选B.
点评:本题的解题关键在于平衡时HI为NH4I分解生成的HI与分解的HI之差,难度较大.

练习册系列答案
相关题目
下列各实验装置图的叙述中,正确的是( )
A、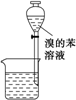 装置①为放出萃取溴水后的苯层 |
B、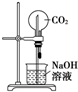 装置②为喷泉实验 |
C、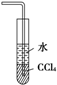 装置③不能用来吸收HCl气体 |
D、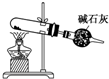 以NH4Cl为原料,装置④可用于制备少量NH3 |
常温下能用铁罐或铝罐贮存的是( )
| A、浓H2SO4 |
| B、浓HCl |
| C、稀H2SO4 |
| D、稀HCl |
高铁电池是一种新型电池,与普通高能电池相比,该电池长时间保持稳定的放电电压.高铁电池的总反应为3Zn+2K2FeO4+8H2O═3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
| A、放电时正极反应为:Zn-2e-+2OH-═Zn(OH)2 |
| B、该原电池,Zn作正极,可用石墨等作负极 |
| C、放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D、放电时正极附近溶液的碱性增强 |
氯碱工业的产物NaOH与不同物质反应可以生成不同的盐.已知常温下,浓度均为0.1mol?L-1的4种钠盐溶液的pH如下表:
下列说法中正确的是( )
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
| A、向氯水中加入NaHCO3溶液,可以增大氯水中次氯酸的浓度 |
| B、四种溶液中,水的电离程度最大的是NaClO |
| C、常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,pH最大的是H2SO3溶液 |
| D、NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>c(OH-) |
某酯的分子式为Cn+4H2n+6O2,它是分子式为CnH2nO的X与有机物Y反应的生成物.有关X、Y的说法正确的是( )
| A、X中一定含有两种官能团:羟基和碳碳双键 |
| B、Y的分子式为C4H6O2,其可能结构有3种 |
| C、Y的分子式为C4H8O2,其属于酯类的结构有4种 |
| D、X和Y都能和碳酸氢钠反应,产生二氧化碳气体 |
下列说法正确的是( )
| A、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出 |
| B、使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干 |
| C、检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
| D、用10mL量筒量取9.2mL NaCl溶液 |
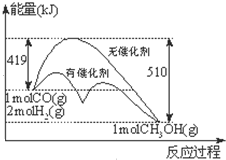 反应CO(g)+2H2(g)?CH3OH(g)过程中能量的变化如图示.下列判断不正确的是( )
反应CO(g)+2H2(g)?CH3OH(g)过程中能量的变化如图示.下列判断不正确的是( )| A、达到平衡时,升高温度,CO的转化率减小 |
| B、1mol CO(g)和2mol H2(g)在密闭容器中反应,达平衡时,放出的热量为91KJ |
| C、相同条件下,1mol CO(g)和2mol H2(g)完全反应生成1mol液态CH3OH放出的热量大于91KJ |
| D、反应热取决于反应物总能量与生成物总能量的相对大小,与反应发生的条件无关 |
利用下列实验装置能完成相应实验的是( )
A、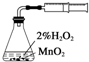 测定化学反应速率 |
B、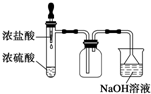 制取并吸收Cl2 |
C、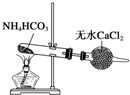 制备纯净的NH3 |
D、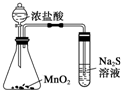 比较MnO2、Cl2、S的氧化性 |