题目内容
3.苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线(如图1):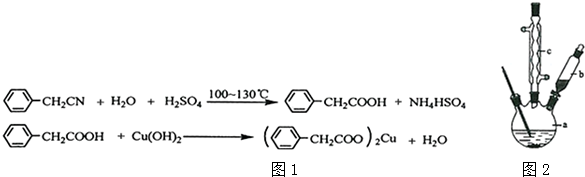
制备苯乙酸的装置示意图如图2(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇.
回答下列问题:
(1)在250mL三口瓶a中加入70mL70%硫酸.配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是先加水,再加浓硫酸.
(2)将a中的溶液加热至100℃,缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应.在装置中,仪器b的作用是滴加苯乙腈;仪器c的名称是球形冷凝管,其作用是回流(或使气化的反应液冷凝).反应结束后加适量冷水,再分离出苯乙酸粗品.加人冷水的目的是便于苯乙酸析出.下列仪器中可用于分离苯乙酸粗品的是BCE(填标号).
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是重结晶,最终得到44g纯品,则苯乙酸的产率是94.6%.
(4)用CuCl2•2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是取少量洗涤液、加入稀硝酸、再加AgNO3溶液、无白色混浊出现.
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是增大苯乙酸溶解度,便于充分反应.
分析 (1)蒸馏水与浓硫酸混合应先加水、再加入浓硫酸,防止暴沸;
(2)仪器b为分液漏斗,通过分液漏斗向三口瓶a中滴加苯乙腈;仪器c为球形冷凝管,能起到冷凝回流的作用(使气化的反应液冷凝);反应结束后加适量冷水,便于苯乙酸(微溶于冷水)结晶析出,通过过滤能从混合液中分离出苯乙酸粗品,过滤所用的仪器主要有漏斗、玻璃棒、烧杯等;
(3)将粗苯乙酸晶体重新在热水中溶解,然后再降温结晶过滤(重结晶)可得较纯净的苯乙酸晶体;
根据“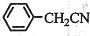 ~
~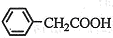 ”关系式计算苯乙酸理论产量,进而计算苯乙酸的产率;
”关系式计算苯乙酸理论产量,进而计算苯乙酸的产率;
(4)在制备Cu(OH)2沉淀的同时还有可溶性NaCl生成,故判断沉淀洗干净的方法就是检验最后一次洗涤液中是否还含有Cl-;
(5)根据“苯乙酸微溶于冷水,溶于乙醇”分析解答.
解答 解:(1)蒸馏水与浓硫酸混合应先加水、再加入浓硫酸,防止暴沸,
故答案为:先加水,再加浓硫酸;
(2)仪器b为分液漏斗,通过分液漏斗向三口瓶a中滴加苯乙腈;仪器c为球形冷凝管,能起到冷凝回流的作用(使气化的反应液冷凝);反应结束后加适量冷水,便于苯乙酸(微溶于冷水)结晶析出,通过过滤能从混合液中分离出苯乙酸粗品,过滤所用的仪器主要有漏斗、玻璃棒、烧杯等,
故答案为:滴加苯乙腈; 球形冷凝管; 回流(或使气化的反应液冷凝);便于苯乙酸析出; BCE;
(3)将粗苯乙酸晶体重新在热水中溶解,然后再降温结晶过滤(重结晶)可得较纯净的苯乙酸晶体;
根据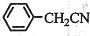 ~
~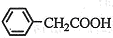 可知,苯乙酸理论产量为$\frac{40g}{117g/mol}$×136g/mol,故苯乙酸的产率=$\frac{44g}{\frac{40g}{117g/mol}×136g/mol}$×1005=94.6%,
可知,苯乙酸理论产量为$\frac{40g}{117g/mol}$×136g/mol,故苯乙酸的产率=$\frac{44g}{\frac{40g}{117g/mol}×136g/mol}$×1005=94.6%,
故答案为:重结晶;94.6%;
(4)在制备Cu(OH)2沉淀的同时还有可溶性NaCl生成,故判断沉淀洗干净的方法就是检验最后一次洗涤液中是否还含有Cl-,具体操作为:取少量洗涤液、加入稀硝酸、再加AgNO3溶液、无白色混浊出现,
故答案为:取少量洗涤液、加入稀硝酸、再加AgNO3溶液、无白色混浊出现;
(5)根据“苯乙酸微溶于冷水,溶于乙醇”,故乙醇与水的混合溶剂中的乙醇能增大苯乙酸的溶解度,便于充分反应,
故答案为:增大苯乙酸溶解度,便于充分反应.
点评 本题考查物质制备实验,综合考查学生实验技能和分析解答问题的能力,题目涉及化学仪器识别、物质分离提纯、实验基本操作等,注意对题目信息的获取与应用,题目难度中等.

| A. | c(HCO3-)=0.1mol•L-1的溶液中:Na+、K+、CO32-、Br- | |
| B. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- | |
| C. | pH=7的溶液中:Al3+、K+、Cl-、SO42- | |
| D. | 使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl- |
| A. | a=b | B. | a<b | C. | a>b | D. | 不能确定 |
| A. | 乙醇在电池的负极上参加反应 | |
| B. | 1mol CH3CH2OH被氧化转移6mole- | |
| C. | 随着反应的进行,正极附近的酸性减弱 | |
| D. | 电池放电过程中化学能转化成电能 |
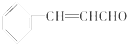
| A. | 煮沸肉桂醛与新制Cu(OH)2的混合物有砖红色沉淀生成 | |
| B. | 电解肉桂醇制得的肉桂醛在电解池的阳极生成 | |
| C. | 仅用新制银氨溶液和溴水不能鉴别肉桂醛中的碳碳双键 | |
| D. | 13.2g肉桂醛分子中含有碳碳双键数目为0.4NA |
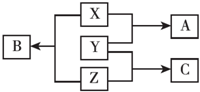 X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16,在适当条件下三种单质两两直接化合,可发生如图所示变化.已知一个B分子中含有Z元素的原子个数比C分子中的Z元素的原子个数少一个.请回答下列问题:
X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16,在适当条件下三种单质两两直接化合,可发生如图所示变化.已知一个B分子中含有Z元素的原子个数比C分子中的Z元素的原子个数少一个.请回答下列问题: ;
; 2NH3;
2NH3;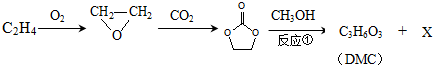
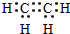 ;石油工业上获得C2H4的操作名称为:石油裂解
;石油工业上获得C2H4的操作名称为:石油裂解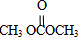

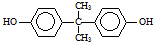 )在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式:
)在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式: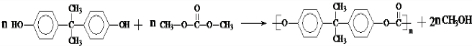 .
.