题目内容
10.下列有关溶液的叙述错误的是( )| A. | pH相同的①CH3COONa、②NaHCO3、③NaAlO2溶液中c(Na+):③>②>① | |
| B. | 将0.2mol•L-1NaHCO3溶液与0.1mol•L-1KOH溶液等体积混合:3c(K+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) | |
| C. | 常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同 | |
| D. | 向AgCl和AgBr的等体积饱和溶液中加入足量AgNO3溶液,则AgCl沉淀多于AgBr沉淀 |
分析 A.酸性CH3COOH>H2CO3>Al(OH)3,酸性越弱,对应盐的水解程度越大;
B.溶液遵循电荷守恒,且c(Na+)=2c(K+);
C.pH=3的CH3COOH溶液和pH=11的NaOH溶液,酸电离的c(H+)═碱电离的c(OH-),对水的抑制程度相同;
D.Ksp(AgCl)>Ksp(AgBr),AgCl和AgBr的等体积饱和溶液中c(Cl-)>c(Br-).
解答 解:A.酸性CH3COOH>H2CO3>Al(OH)3,酸性越弱,对应盐的水解程度越大,等浓度时③的pH最大,则pH相同的①CH3COONa、②NaHCO3、③NaAlO2溶液中c(Na+):③<②<①,故A错误;
B.溶液中电荷守恒式为c(Na+)+c(K+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-),且c(Na+)=2c(K+),则3c(K+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-),故B正确;
C.pH=3的CH3COOH溶液和pH=11的NaOH溶液,酸电离的c(H+)═碱电离的c(OH-),对水的抑制程度相同,则水的电离程度相同,故C正确;
D.Ksp(AgCl)>Ksp(AgBr),AgCl和AgBr的等体积饱和溶液中c(Cl-)>c(Br-),则加入足量AgNO3溶液,AgCl沉淀多于AgBr沉淀,故D正确;
故选A.
点评 本题考查难溶电解质、盐类水解,为高频考点,把握盐类水解规律、电荷守恒、Ksp及溶解平衡移动为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.相同质量的下列各烃,完全燃烧后生成CO2最多的是( )
| A. | 甲烷 | B. | 乙烯 | C. | 苯 | D. | 乙烷 |
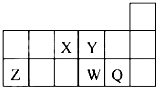
1.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )

| A. | 元素X与元素Z的正化合价之和的数值等于8 | |
| B. | 原子半径的大小顺序为rX>rY>rZ>rW>rQ | |
| C. | Y和Z形成了共价化合物 | |
| D. | 元素W周期表中的位置是第三周期,第VI主族 |
18.下面有关Fe(OH)3胶体的说法错误的是( )
| A. | Fe(OH)3胶体可用将FeCl3饱和溶液滴入沸水的方法来制备 | |
| B. | Fe(OH)3胶体电泳时,可以观察到阳极颜色加深 | |
| C. | 向 Fe(OH)3胶体中逐滴滴加稀盐酸,现象是先产生红褐色沉淀后沉淀溶解 | |
| D. | 不断搅拌Fe(OH)3胶体,溶液会变浑浊 |
5.氯碱工业中电解饱和食盐水的原理示意图如图所示(电极均为石墨电极).下列说法正确的是( )

| A. | M为电子流出的一极 | |
| B. | 通电使氯化钠发生电离 | |
| C. | 电解一段时间后,阴极区pH降低 | |
| D. | 电解时用盐酸调节阳极区的pH在2~3,有利于气体逸出 |
19.下列有关环境污染的叙述错误的是( )
| A. | 酸雨通常是指pH在7以下的降水 | |
| B. | 氮氧化物是造成光化学烟雾的主要原因 | |
| C. | 大气污染主要指CO、SO2、氮氧化物以及粉尘等 | |
| D. | N与S的氧化物直接危害人的身体健康,引发呼吸道疾病 |
20.100mL 6mol•L-1的硫酸溶液与过量锌粉反应,在一定温度下为了减缓反应速率但又不影响生成氢气的总质量,可向反应物中加入适量的( )
| A. | 硝酸 | B. | 水 | C. | 硫酸氢钾 | D. | 氯化氢气体 |
 或
或 .
.