题目内容
1.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )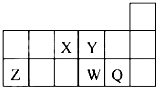
| A. | 元素X与元素Z的正化合价之和的数值等于8 | |
| B. | 原子半径的大小顺序为rX>rY>rZ>rW>rQ | |
| C. | Y和Z形成了共价化合物 | |
| D. | 元素W周期表中的位置是第三周期,第VI主族 |
分析 由短周期元素X、Y、Z、W、Q在元素周期表中的相对位置可知,X为N,Y为O,Z为Al,W为S,Q为Cl,
A.元素X与元素Z的正化合价分别为+5、+3;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小;
C.Y和Z形成化合物为氧化铝;
D.W的最外层电子数为6.
解答 解:由短周期元素X、Y、Z、W、Q在元素周期表中的相对位置可知,X为N,Y为O,Z为Al,W为S,Q为Cl,
A.元素X与元素Z的正化合价分别为+5、+3,则正化合价之和的数值等于8,故A正确;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径为rZ>rW>rQ>rX>rY,故B错误;
C.Y和Z形成化合物为氧化铝,含离子键,为离子化合物,故C错误;
D.W的最外层电子数为6,位于第三周期ⅥA族,故D错误;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、元素的性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
11.下列电离方程式中,不正确的是( )
| A. | H2O+H2O?H3O++OH- | B. | NH3•H2O═NH4++OH- | ||
| C. | CH3COOH?CH3COO-+H+ | D. | Na2CO3═2Na++CO32- |
12.下列金属氧化物的水化物碱性最强的是( )
| A. | CsOH | B. | Al(OH)3 | C. | NaOH | D. | Mg(OH)2 |
9.NA代表阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,7g乙烯(C2H4)与丙烯(C3H6)混合气体含有的氢原子数为NA | |
| B. | 标准状况下22.4L一氯甲烷和二氯甲烷的混合物中所含氯原子数介于NA至2NA之间 | |
| C. | lmol FeCl2与足量氯气反应时转移的电子数为2NA | |
| D. | 0.2 mol/L的Na2S溶液中,所含S2-数目小于 0.2NA |
16.向含有下列离子的各组溶液中分别通入一定量相应气体,各离子还能大量存在的是( )
| A. | Cu2+、SO42-,通硫化氢 | B. | Na+、S2O32-,通氯化氢 | ||
| C. | Ba2+、C1-,通二氧化硫 | D. | Ba2+、NO3-,通二氧化硫 |
6.有机物甲分子式为C11H14O2,在酸性条件下水解生成乙和丙,丙遇FeCl3溶液显色,丙的相对分子质量比乙大20,甲的结构有( )
| A. | 3种 | B. | 4种 | C. | 8 种 | D. | 6 种 |
13.下列各组元素性质或原子结构的递变,叙述不正确的是( )
| A. | Na、Mg、Al最高价氧化物的水化物碱性逐渐减弱 | |
| B. | P、S、Cl得电子能力依次增强 | |
| C. | Li、Na、K的密度依次增大 | |
| D. | C、N、O元素气态氢化物稳定性增强 |
10.下列有关溶液的叙述错误的是( )
| A. | pH相同的①CH3COONa、②NaHCO3、③NaAlO2溶液中c(Na+):③>②>① | |
| B. | 将0.2mol•L-1NaHCO3溶液与0.1mol•L-1KOH溶液等体积混合:3c(K+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) | |
| C. | 常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同 | |
| D. | 向AgCl和AgBr的等体积饱和溶液中加入足量AgNO3溶液,则AgCl沉淀多于AgBr沉淀 |
11.能用KMnO4溶液而不能用溴水鉴别的是( )
| A. | 甲烷和乙烯 | B. | 1,3-丁二烯和丁烯 | ||
| C. | 苯和丙苯 | D. | 氢氧化钠溶液和苯酚溶液 |