题目内容
20.关于有机物 的说法不正确的是( )
的说法不正确的是( )| A. | 有机物的分子式是C10H18O | B. | 能与溴水、钠发生反应 | ||
| C. | 能发生氧化、取代反应 | D. | 与HC1发生加成的产物只有1种 |
分析 有机物含有碳碳双键、羟基,结合烯烃、醇的性质解答该题.
解答 解:A.有结构简式可知有机物的分子式是C10H18O,故A正确;
B.含有碳碳双键,可与溴水发生加成反应,含有羟基,可与钠反应,故B正确;
C.含有碳碳双键,可发生氧化反应,含有羟基,可发生取代反应,故C正确;
D.含有碳碳双键,且结构不对称,则与HC1发生加成的产物有2种,故D错误.
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
11.下列指定反应的离子方程式正确的是( )
| A. | Cl2通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O | |
| C. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| D. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
8.向盛有10mLlmol/LNH4Al(SO4)2溶液的烧杯中滴加1mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如图.下列有关说法正确的是( )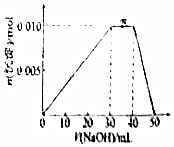

| A. | 当加入50mLNaOH时,溶液中的溶质为NaAlO2 | |
| B. | m点反应的离子方程式:NH4++OH-═NH3•H2O | |
| C. | NH4Al(SO4)2溶液中离子浓度由大到小的顺序是:c(SO42-)>c(Al3+)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 若向NH4Al(SO4)2溶液改加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为0.02mol |
15.下列有关说法不正确的是( )
| A. | 反应SiO2(s)+3C(s)═SiC(s)+2CO(g)室温下不能自发进行,则该反应的△H>0 | |
| B. | 等pH的CH3COOH、HCl溶液混合后,平衡不移动,但c(CH3COO-)减少 | |
| C. | 配制KF溶液时,必需要加入KOH溶液抑制F-水解 | |
| D. | 向NaHS溶液中滴入少量CuCl2溶液产生黑色沉淀,HS-电离程度增大,pH减小 |
12.下列能源不属于一次能源的是( )
| A. | 风力 | B. | 石油 | C. | 流水 | D. | 电力 |
9.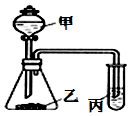 利用如图所示装置,采用适当试剂可完成下表的探究实验,并得出相应的实验结论,其中错误的是( )
利用如图所示装置,采用适当试剂可完成下表的探究实验,并得出相应的实验结论,其中错误的是( )
 利用如图所示装置,采用适当试剂可完成下表的探究实验,并得出相应的实验结论,其中错误的是( )
利用如图所示装置,采用适当试剂可完成下表的探究实验,并得出相应的实验结论,其中错误的是( )| 选项 | 甲 | 乙 | 丙 | 装置丙中的现象 | 实验结论 |
| A | 稀硝酸 | 碳酸钾 | 澄淸石灰水 | 变浑浊 | 酸性:HNO3>H2CO3 |
| B | 稀硫酸 | 碳酸钠 | 次氯酸钙溶液 | 白色沉淀 | 酸性:H2CO3>HClO |
| C | 浓盐酸 | 大理石 | 硅酸钠溶液 | 白色沉淀 | 非金属性:C>Si |
| D | 浓盐酸 | 高锰酸钾 | 石蕊溶液 | 先变红后褪色 | 氯水既有酸性,又具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
10.利用如图所示装置进行实验,能实现实验目的是(必要时可加热)( )
| 选项 | 实验目的 | 甲 | 乙 | 丙 | 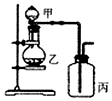 |
| A | 证明浓硫酸具有强氧化性 | 浓硫酸 | 碳粉 | 溴水 | |
| B | 验证Cl2无漂白性 | 浓盐酸 | MnO2 | 干燥的红色布条 | |
| C | 验证NH3溶于水显碱性 | 浓氨水 | 碱石灰 | 湿润的蓝色石蕊试纸 | |
| D | 比较H2CO3和H2SiO3的酸性 | 硼酸溶液 | 碳酸钠 | 硅酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |