��Ŀ����
8�������Ƕ���Ҫ�������仯��������ۣ�����Ҫ��ش����⣺��1��д������ˮ��Ӧ�����ӷ���ʽ2Na+2H2O=2Na++2OH-+H2����Na2O2����;֮һ��DZˮͧ�����������������������Դ��
��2����AlCl3��Һ����ε��������NaOH��Һ���۲쵽���������ȳ������ܽ⣬��Ӧ�����ӷ���ʽΪAl3++3OH-=3Al��OH��3����Al��OH��3+OH-=AlO2-+2H2O��
��3�����ֱ���������NaOH��Һ��ϡ���ᷴӦ����������Ӧ����ͬ״���·ų����������壬��������Ӧ�����ĵ��������ʵ���֮��Ϊ1��1��
���� ��1������ˮ��Ӧ�����������ƺ�����������������ˮ��������̼��Ӧ������������
��2���Ȼ������������Ʒ�Ӧ�������������������������������������������Ʒ�Ӧ����ƫ�����ƣ�
��3��������ת�Ƶ����غ���㣮
��� �⣺��1������ˮ��Ӧ�����������ƺ����������ӷ���ʽ��2Na+2H2O=2Na++2OH-+H2��������������ˮ��������̼��Ӧ����������������DZˮͧ�����������������������Դ��
�ʴ�Ϊ��2Na+2H2O=2Na++2OH-+H2����DZˮͧ���������������������Դ��
��2���Ȼ������������Ʒ�Ӧ�������������������������������������������Ʒ�Ӧ����ƫ�����ƣ����ӷ���ʽ�ֱ�Ϊ��Al3++3OH-=3Al��OH��3�� Al��OH��3+OH-=AlO2-+2H2O������Ϊ���ȳ������ܽ⣻
�ʴ�Ϊ���ȳ������ܽ⣻Al3++3OH-=3Al��OH��3���� Al��OH��3+OH-=AlO2-+2H2O��
��3�����ֱ���������������ƺ�ϡ���ᷴӦ�����������ͬ�����µ�������������������Ӧ�ж�����ʧ���ӣ���ת�Ƶ����غ�֪����Ҫ�������ʵ���֮��Ϊ1��1��
�ʴ�Ϊ��1��1��
���� ���⿼�������ӷ���ʽ����д�����ݷ���ʽ�ļ����֪ʶ�㣬��ȷ���ӷ���ʽ����д�����ǽⱾ��ؼ����ٽ��ת�Ƶ����غ���м��㣬��Ŀ�ѶȲ���

| A�� | ���ʹ��ǹ��ά����Ҫ�ɷ� | B�� | ��������������ˮɱ������ | ||
| C�� | ��������������ɫ�����Ϳ�� | D�� | �������ƿ�����DZͧ����������Դ |
| A�� | Ũ�����Ũ���������ǿ������ | |
| B�� | Ũ�����Ũ���᳤��¶���ڿ�����Ũ�Ⱦ������� | |
| C�� | ������Ũ�����Ũ����������������������� | |
| D�� | Ũ�����Ũ���᳣���¾�������CuѸ�ٷ�Ӧ |
| A�� | Na��Mg��AlԪ������ϼ��������� | B�� | P��S��Clԭ�Ӱ뾶���μ�С | ||
| C�� | N��O��FԪ�طǽ��������μ��� | D�� | Li��Na��Kԭ�ӵĵ��Ӳ����������� |
| A�� | ����������Һ�����ڴ���Ƥ���IJ����Լ�ƿ�� | |
| B�� | Ư�۳��ڷ������ձ��� | |
| C�� | FeSO4��Һ����ڼ����������۵��Լ�ƿ�� | |
| D�� | �������Ʊ�����ú���� |
| A�� | ͬŨ��������Һ�У��٣�NH4��2SO4 ��NH4HCO3 ��NH4Cl ��NH3•H2O��c��NH4+���ɴ�С��˳���ǣ��ܣ��ۣ��ڣ��� | |
| B�� | ����ʱ���������������Ͱ�ˮ��Ϻ�pH=7����c ��NH4+����c ��Cl-�� | |
| C�� | 0.2 mol•L-1Na2CO3��Һ�У�c ��CO32-��+c ��HCO3-��+c ��H2CO3��=0.2 mol•L-1 | |
| D�� | ���������Һ�м����������ᣬ�õ�������Һ��c��Na+����c��CH3COO-����c��H+����c��OH-�� |
| A�� | ��֪C2H6��ȼ����Ϊ1090 kJ•mol-1����C2H6ȼ�յ��Ȼ�ѧ����ʽΪ��C2H6��g��+3.5O2��g���T2CO2��g��+3H2O��g����H=-1090 kJ/mol | |
| B�� | 25�棬101kPa�£�l mol C6H6ȼ������CO2��Һ̬ˮʱ�ų�3260 kJ���������Ȼ�ѧ����ʽΪ��C6H6��g��+7.5O2��g��=6CO2��g��+3H2O ��l����H=-3260kJ•mol-1 | |
| C�� | ��֪�����£�H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ/mol����ϡ������ϡNaOH��Һ��Ӧ����1 mol H2O��l��ʱҲ�ų�57.3 kJ������ | |
| D�� | ��֪2CO��g��+O2��g���T2CO2��g����H=-566 kJ•mol-1����CO��ȼ����233kJ•mol-1 |
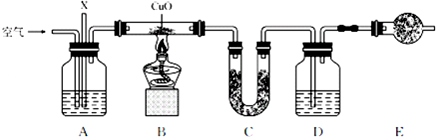
��1����Aװ������ʢ�ŵ�ҩƷ��ŨNaOH ��Һ��װ��A�������У�
�ٳ�ȥ�����е�CO2���壻
�ڵ���X�Ϳ�����ͨ�����ʣ���֤O2����
��2��Dװ������ʢ�ŵ�ҩƷ��ŨNaOH��Һ��
��3��Eװ�õ������Ƿ�ֹ�����еĶ�����̼��ˮ��������װ��D���Խ������Ӱ�죬
��4������װ������һ��ȱ�ݣ��������A��B֮���һ��ʢŨ�����ϴ��ƿ��ʢ��ˮCaCl2����P2O5����ʯ�ҡ�����NaOH�ȣ��ĸ���ܣ�
��5����ʵ��װ�þ��������õ���ʵ���������£�
| ���� | ʵ��ǰ | ʵ��� |
| ҩƷ+U�ιܵ�����/g | 101.1 | 102.9 |
| ҩƷ+���ƿD������/g | 312.0 | 314.2 |