题目内容
3.干冰是( )①单质;②混合物;③化合物;④纯净物;⑤氧化物.
| A. | ①②③ | B. | ②③④⑤ | C. | ①③⑤ | D. | ③④⑤ |
分析 ①单质是一种元素组成的纯净物;
②混合物是不同物质组成的物质;
③化合物不同元素组成的纯净物;
④纯净物一种物质组成的物质;
⑤氧化物,两种元素组成其中一种为氧元素的化合物为氧化物;
干冰是固体二氧化碳,是一种物质组成的纯净物,二氧化碳由不同元素组成的纯净物为化合物.
解答 解:干冰是固体二氧化碳,是一种物质组成的纯净物,二氧化碳由不同元素组成的纯净物为化合物,两种元素组成其中一种为氧元素的化合物为氧化物,二氧化碳是化合物、纯净物、氧化物,故选D.
点评 本题考查了物质分类、物质组成,主要是概念的理解应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
13.已知Mg(OH)2的溶解度大于Fe(OH)3的溶解度.要除去混在MgCl2溶液中的FeCl3,可以边搅拌边加入一种试剂,这种试剂是( )
| A. | Na2CO3 | B. | NaOH | C. | Mg(OH)2 | D. | NH3•H2O |
14.属于氧化还原反应的离子方程式的是( )
| A. | CaCO3+2H+=Ca2++CO2↑+H2O | B. | 2Fe2++Cl2=2Fe3++2Cl- | ||
| C. | HCO3-+H+=CO2↑+H2O | D. | H++OH-=H2O |
11.下列说法中正确的是( )
| A. | 在电解池中,物质在阴极发生氧化反应 | |
| B. | 在电解池中,与电源正极相连的电极是阴极 | |
| C. | 在原电池中,物质在负极发生氧化反应 | |
| D. | 在原电池中,电子由正极流向负极 |
18.下列叙述正确的是( )
| A. | 酸性氧化物不一定都是非金属氧化物 | |
| B. | HCl、H2S、NH3都是电解质 | |
| C. | 强酸强碱都是离子化合物 | |
| D. | FeBr3、FeCl2、CuS都不能直接用化合反应制备 |
8.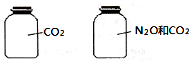 如图所示,两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不发生化学反应)的关系不一定正确的是( )
如图所示,两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不发生化学反应)的关系不一定正确的是( )
 如图所示,两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不发生化学反应)的关系不一定正确的是( )
如图所示,两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不发生化学反应)的关系不一定正确的是( )| A. | 所含氧原子数相等 | B. | 气体的总质量相等 | ||
| C. | 气体所含电子总数相等 | D. | 气体的密度相等 |
15.氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应中属于区域3的是( )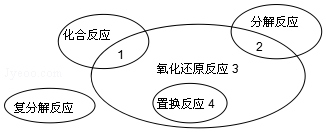

| A. | 2K2O2+2CO2═2K2CO3+O2 | B. | Cl2+2KBr═Br2+2KCl | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2NaHCO3═Na2CO3+H2O+CO2↑ |
9.已知常温下Ksp(AgCl)=1.6×10-10、Ksp(AgI)=2.0×10-16,下列说法中正确的是( )
| A. | 含有大量Cl-的溶液中肯定不存在Ag+ | |
| B. | AgI悬浊液中加入少量KI粉末,平衡AgI(s)?Ag+(aq)+I-(aq)向左移动,溶液中离子的总浓度会减小 | |
| C. | AgCl悬浊液中逐渐加入KI固体至c(I-)=$\frac{{K}_{sp}(AgI)}{{K}_{sp}(AgCl)}$mol•L-1时,AgCl开始向AgI沉淀转化 | |
| D. | 向浓度均为0.01 mol•L-1的KCl和KI的混合溶液中滴加AgNO3溶液,当Cl-开始沉淀时,溶液中I-的浓度为1.25×10-8 mol•L-1 |