题目内容
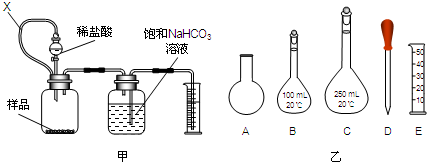
 如图1所示是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
如图1所示是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:(1)从氯化钾溶液中得到氯化钾固体选择装置
(2)从碘水中分离出I2,选择装置
(3)装置A中①的名称是
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如图2流程的实验:

问题1:粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用.粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加入盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发.正确的操作顺序是
a.⑤②③①④⑥⑦b.⑤①②③⑥④⑦c.⑤②①③④⑥⑦d. ⑤③②①⑥④⑦
问题2:按所选顺序操作时,步骤④的化学方程式是
问题3:由海水到氯化钠晶体的实验过程中要用到的主要装置是
考点:物质分离和提纯的方法和基本操作综合应用,物质分离、提纯的实验方案设计
专题:实验设计题
分析:(1)从溶液中得到固体采用蒸发结晶的方法;除去自来水中的Cl-等杂质采用蒸馏的方法;
(2)从碘水中分离出I2,碘易溶于有机溶剂而难溶于水,所以可以采用萃取方法;
(3)装置A中①的名称是冷凝管,进水的方向是“下进上出”;
(4)问题1.粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,提纯过程中,先加水溶解,然后把杂质转化为沉淀或气体除去,除Ca2+用CO32-,除Mg2+、Fe3+用OH-,除SO42-用Ba2+.要注意除杂质的顺序,后加的试剂最好能把前面先加的过量试剂除掉;
问题2:原来溶液中存在NaOH、Na2CO3,加入HCl后,HCl和NaOH、Na2CO3发生反应生成NaCl;
问题3:由海水到氯化钠晶体的实验过程中先沉淀杂质离子,然后过滤最后蒸发浓缩.
(2)从碘水中分离出I2,碘易溶于有机溶剂而难溶于水,所以可以采用萃取方法;
(3)装置A中①的名称是冷凝管,进水的方向是“下进上出”;
(4)问题1.粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,提纯过程中,先加水溶解,然后把杂质转化为沉淀或气体除去,除Ca2+用CO32-,除Mg2+、Fe3+用OH-,除SO42-用Ba2+.要注意除杂质的顺序,后加的试剂最好能把前面先加的过量试剂除掉;
问题2:原来溶液中存在NaOH、Na2CO3,加入HCl后,HCl和NaOH、Na2CO3发生反应生成NaCl;
问题3:由海水到氯化钠晶体的实验过程中先沉淀杂质离子,然后过滤最后蒸发浓缩.
解答:
解:(1)从溶液中得到固体采用蒸发结晶的方法,所以从KCl溶液中得到KCl固体采用蒸发结晶的方法;氯离子易溶于水,但难挥发,水易被蒸发,所以除去自来水中的Cl-等杂质采用蒸馏的方法,
故答案为:D;A;
(2)从碘水中分离出I2,碘易溶于有机溶剂而难溶于水,所以可以采用萃取方法将碘从碘水中提取,然后采用分液方法分离,故答案为:B;萃取、分液;
(3)装置A中①的名称是冷凝管,进水的方向是“下进上出”,否则水蒸气急剧冷却易产生爆炸,故答案为:冷凝管;下口进水;
(4)问题1.去粗盐中的可溶性杂质:Mg2+、Ca2+、Fe3+、SO42-时,先加水溶解,所以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;
加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,氢氧化钠和氯化钡可以颠倒加入的顺序,然后过滤,最后调节溶液的pH等于7后蒸发即可,
所以其顺序是⑤③②①⑥④⑦,故选d;
问题2:原来溶液中存在NaOH、Na2CO3,加入HCl后,HCl和NaOH、Na2CO3发生反应生成NaCl,发生的反应为HCl+NaOH=NaCl+H2O、2HCl+Na2CO3=2NaCl+H2O+CO2↑,故答案为:HCl+NaOH=NaCl+H2O,2HCl+Na2CO3=2NaCl+H2O+CO2↑;
问题3:由海水到氯化钠晶体的实验过程中先沉淀杂质离子,然后过滤最后蒸发浓缩,所以需要过滤和蒸发装置,故选CD.
故答案为:D;A;
(2)从碘水中分离出I2,碘易溶于有机溶剂而难溶于水,所以可以采用萃取方法将碘从碘水中提取,然后采用分液方法分离,故答案为:B;萃取、分液;
(3)装置A中①的名称是冷凝管,进水的方向是“下进上出”,否则水蒸气急剧冷却易产生爆炸,故答案为:冷凝管;下口进水;
(4)问题1.去粗盐中的可溶性杂质:Mg2+、Ca2+、Fe3+、SO42-时,先加水溶解,所以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;
加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,氢氧化钠和氯化钡可以颠倒加入的顺序,然后过滤,最后调节溶液的pH等于7后蒸发即可,
所以其顺序是⑤③②①⑥④⑦,故选d;
问题2:原来溶液中存在NaOH、Na2CO3,加入HCl后,HCl和NaOH、Na2CO3发生反应生成NaCl,发生的反应为HCl+NaOH=NaCl+H2O、2HCl+Na2CO3=2NaCl+H2O+CO2↑,故答案为:HCl+NaOH=NaCl+H2O,2HCl+Na2CO3=2NaCl+H2O+CO2↑;
问题3:由海水到氯化钠晶体的实验过程中先沉淀杂质离子,然后过滤最后蒸发浓缩,所以需要过滤和蒸发装置,故选CD.
点评:本题考查物质的分离和提纯,明确物质的性质是解本题关键,知道常见物质的分离方法,根据物质性质选取合适的分离方法,难点是除杂剂滴加先后顺序,题目难度中等.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
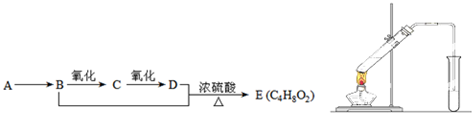
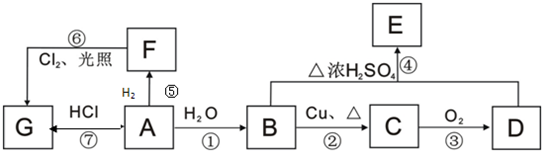
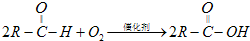 (R表示烃基),请回答下列问题:
(R表示烃基),请回答下列问题: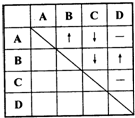 为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成.).
为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成.).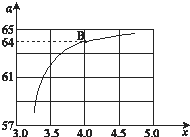 工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下: