题目内容
3.等质量的CO2、SO2,它们的原子个数比为11:16.分析 根据n=$\frac{N}{N{\;}_{A}}$=$\frac{m}{M}$结合二氧化碳、二氧化硫为三原子分子结构解答.
解答 解:根据n=$\frac{m}{M}$可知,质量的SO2气体和CO2气体的物质的量之比为44g/mol:64g/mol=11:16,每个分子均含有3个原子,则二者含有原子数目之比为11:16,
故答案为:11:16.
点评 本题考查物质的量的有关计算,为高频考点,明确以物质的量为核心计算公式是解题关键,注意物质的结构组成,题目难度不大.

练习册系列答案
相关题目
13.相等物质的量的CO和CO2,下列比较中正确的是( )
①所含的分子数目之比为1:1 ②所含的氧原子数目之比为1:2
③所含的碳原子数目之比为1:1 ④所含的原子总数目之比为2:3.
①所含的分子数目之比为1:1 ②所含的氧原子数目之比为1:2
③所含的碳原子数目之比为1:1 ④所含的原子总数目之比为2:3.
| A. | ①② | B. | ②③ | C. | ①②③ | D. | ①②③④ |
14.硅及其化合物在材料领域中应用广泛.下列叙述中,正确的是( )
| A. | 用带玻璃瓶塞的试剂瓶盛放NaOH溶液 | |
| B. | 硅是地壳中含量最多的元素 | |
| C. | SiO2不溶于水,也不溶于任何酸 | |
| D. | 晶体硅是良好的半导体材料 |
11.下列生产或实验事实得出的相应结论不正确的是( )
| 选项 | 事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| B | A、B两支试管,各加入4mL0.01mol/L的KMnO4酸性溶液,在A试管中加入2mL0.01mol/LH2C2O4溶液和在B试管中加入4mL 0.02mol/L的H2C2O4溶液,记录溶液褪色所需时间,B试管褪色时间短 | 当其他条件不变时,增大反应物浓度,化学反应速率加快 |
| C | 在容积可变的密闭容器中发生反应:2NH3(g)?N2H4(l)+H2(g),把容器的体积缩小一半 | 正反应速率加快,逆反应速率减慢 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A. | A | B. | B | C. | C | D. | D |
18.配制一定量浓度的NaOH溶液,下列操作正确的是( )
| A. | 称量时,将NaOH固体放在右盘,砝码放在左盘 | |
| B. | 将NaOH固体在烧杯中溶解,所得的溶液冷却至室温后,再转移到容量瓶中 | |
| C. | 转移液体时,可以不用将洗涤液转至容量瓶 | |
| D. | 定容时,可以俯视刻度线读数 |
15.如图是某同学用500mL容量瓶配制0.10mol•L-1 Na2CO3溶液的步骤:该同学的错误是( )
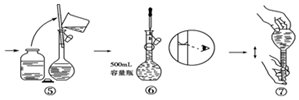

| A. | ⑤⑥ | B. | ⑦ | C. | ⑥ | D. | ⑤⑥⑦ |
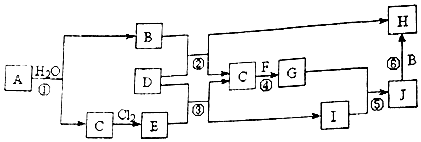
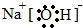 .
.