题目内容
某无色酸性溶液中可能存在的一组离子是( )
| A、K+、SO42-、Al3+、Cl- |
| B、Na+、Cu2+、NO3-、Cl- |
| C、Na+、CO32-、SO42-、Mg2+ |
| D、Ag+、NO3-、K+、Br-- |
考点:离子共存问题
专题:离子反应专题
分析:酸性溶液中含大量的H+,根据离子之间不能结合生成沉淀、气体、弱电解质等,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答:
解:A.酸性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故A选;
B.酸性溶液中该组离子之间不反应,可大量共存,但Cu2+为蓝色,与无色溶液不符,故B不选;
C.CO32-、Mg2+结合生成沉淀,CO32-、H+结合水和气体,不能共存,故C不选;
D.Ag+、Br-结合生成沉淀,不能大量共存,故D不选;
故选A.
B.酸性溶液中该组离子之间不反应,可大量共存,但Cu2+为蓝色,与无色溶液不符,故B不选;
C.CO32-、Mg2+结合生成沉淀,CO32-、H+结合水和气体,不能共存,故C不选;
D.Ag+、Br-结合生成沉淀,不能大量共存,故D不选;
故选A.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
将等质量的镁铝混合分成四等分,分别加入到足量下列溶液中,充分反应后放出氢气体最多的是( )
| A、3mol?L-1的HCl |
| B、4mol?L-1的HNO3 |
| C、8mol?L-1的NaOH |
| D、18mol?L-1的H2SO4 |
常温下,下列关于电解质溶液的正确判断是( )
| A、pH=11的NaOH溶液中c(H+)是pH=9的Ba(OH)2溶液中c(H+)的100倍 |
| B、使甲基橙变红的溶液中,K+、NO3-、SO32-、HCO3-可以大量共存 |
| C、由0.1 mol?L-1一元酸HA溶液的pH=1,可推知HA溶液存在HA?H++A- |
| D、由0.1 mol?L-1一元碱MOH溶液的pH=10,可推知MCl溶液pH<7 |
某盐的混合溶液中,含有Na+0.3mol、Al3+ 0.3mol、SO42-0.4mol,则该盐中含有Cl-的物质的量是( )
| A、0.2mol |
| B、0.4mol |
| C、0.6mol |
| D、0.8mol |
下列说法中不正确的是( )
| A、CH3CBr(OH)CH2OH是手性分子 |
| B、HF、HCl、HBr、HI的热稳定性依次减弱 |
| C、F2、C12、Br2、I2的熔、沸点逐渐升高 |
| D、邻羟基苯甲醛的熔点比对羟基苯甲醛高 |
下列各组物质的成分完全相同的是( )
| A、液氯和氯气 |
| B、液氯和氯水 |
| C、氯化氢和盐酸 |
| D、水煤气和天然气 |
下列物质水溶液经加热浓缩、蒸干后适当加热不能得到原物质的是( )
①NH4HCO3; ②CaCl2; ③AlCl3; ④Cu(NO3)2; ⑤FeCl2;⑥K2SO3; ⑦KMnO4; ⑧KAl(SO4)2.
①NH4HCO3; ②CaCl2; ③AlCl3; ④Cu(NO3)2; ⑤FeCl2;⑥K2SO3; ⑦KMnO4; ⑧KAl(SO4)2.
| A、①③④⑤⑥⑦ | B、①②③⑤ |
| C、①③④⑤ | D、以上均不能 |
用下列实验装置进行相应实验,能达到实验目的是( )
A、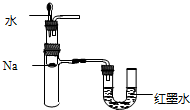 验证Na和水反应放热 |
B、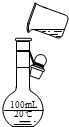 将溶液定容到100mL |
C、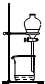 分离酒精和水 |
D、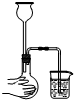 检查装置的气密性 |