题目内容
用下列实验装置进行相应实验,能达到实验目的是( )
A、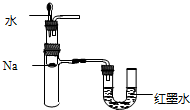 验证Na和水反应放热 |
B、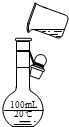 将溶液定容到100mL |
C、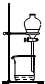 分离酒精和水 |
D、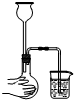 检查装置的气密性 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.根据U形管内液体的液面变化可判断反应是吸热反应还是放热反应;
B.缺少玻璃棒;
C.乙醇和水能互溶;
D.长颈漏斗中应加入水.
B.缺少玻璃棒;
C.乙醇和水能互溶;
D.长颈漏斗中应加入水.
解答:
解:A.钠和水的反应为放热反应,反应后试管内温度升高,压强增大,U形管左端液面下降,故A正确;
B.转移液体需要用玻璃棒引流,故B错误;
C.乙醇和水能互溶,不分层,不能用分液漏斗分离,故C错误;
D.长颈漏斗中应加入水,超过漏斗下端,故D错误.
故选A.
B.转移液体需要用玻璃棒引流,故B错误;
C.乙醇和水能互溶,不分层,不能用分液漏斗分离,故C错误;
D.长颈漏斗中应加入水,超过漏斗下端,故D错误.
故选A.
点评:本题考查较为综合,侧重于物质性质实验方案的设计和实验方案的评价,注意把握物质的性质,易错点为D,注意掌握气密性的方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某无色酸性溶液中可能存在的一组离子是( )
| A、K+、SO42-、Al3+、Cl- |
| B、Na+、Cu2+、NO3-、Cl- |
| C、Na+、CO32-、SO42-、Mg2+ |
| D、Ag+、NO3-、K+、Br-- |
将Na2O2投入到FeCl2溶液中可观察到的现象是( )
| A、生成白色沉淀 |
| B、生成红褐色沉淀 |
| C、溶液变为棕黄色 |
| D、无气体生成 |
下列说法正确的是( )
| A、含有金属阳离子的晶体一定是离子晶体 |
| B、固态和熔融状态可导电,投入水中形成的水溶液也可导电,该物质可能是金属晶体 |
| C、白磷晶体中只存在一种作用力,即分子间作用力 |
D、如图,NaCl晶体中,距离最近的Na+组成的最小多面体是正八面体 |
在金属钠与水反应的实验中不能反映出钠的性质是( )
| A、良导体 | B、还原性强 |
| C、密度小 | D、熔点低 |
已知NH3极易溶于水,下列组合中不能形成喷泉的是( )
| A、HCl和H2O |
| B、O2和H2O |
| C、NH3和H2O |
| D、CO2和NaOH |
下列实验中,所选装置不合理的是( )


| A、粗盐提纯,选①和② |
| B、用CCl4提取碘水中的碘,选③ |
| C、分离Na2CO3溶液和CH3COOC2H5,选④ |
| D、用NaOH溶液吸收Cl2,选⑤ |
物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )
| A、Ba(OH)2、Na2SO3、FeCl3、KCl |
| B、Na2CO3、NaHCO3、KNO3、NH4Cl |
| C、NH3?H2O、H3PO4、Na2SO4、H2SO4 |
| D、HCl、CH3COOH、C2H5OH、Na2SiO3 |
用NA表示阿伏加德罗常数的值,下列叙述错误的是( )
| A、含有NA个氢原子的氢气在标准状况下的体积约为11.2L |
| B、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| C、在常温常压下,35.5g Cl2含有的分子数为0.5NA |
| D、标准状况下,11.2L H2O含有的分子数为0.5NA |