题目内容
15.在一定条件下,氯气可与氯化铵发生如下反应:xCl2+NH4Cl═yNClx+(x+y)HCl,当消耗6.72L标准状况下的Cl2时,生成0.100mol氮的氯化物,则此氮的氯化物的化学式为( )| A. | NCl2 | B. | NCl3 | C. | NCl4 | D. | NCl5 |
分析 先根据得失电子配平方程式,再根据氯气和氮的氯化物之间的关系式计算得出n从而确定化学式.
解答 解:xCl2+yNH4Cl→yNCln+(x+y)HCl,根据氧化还原反应中得失电子数相等配平该方程式,
(n+3)Cl2+2NH4Cl=2NCln+8HCl
n+3 2
$\frac{6.72L}{22.4L/mol}$ 0.10mol
所以n=3,该氯化物的化学式为NCl3,
故选B.
点评 本题考查氧化还原的计算,题目难度不大,本题注意氨气并没有全部被氧化,比较容易.

练习册系列答案
相关题目
2.下列离子方程式正确的是( )
| A. | 铁与稀硫酸反应 Fe+2H+═Fe3++H2↑ | |
| B. | 氢氧化铝与足量盐酸反应 Al(OH)3+3H+═Al3++3H2O | |
| C. | 钠和冷水反应 Na+2H2O═Na++H2↑+OH- | |
| D. | 铜片与稀硝酸反应 Cu+NO3-+4H+═Cu2++NO↑+2H2O |
10.用NA表示阿伏德罗常数,下列叙述错误的是( )
| A. | 28g N2所含原子数为NA | B. | 0.5mol H2O所含原子数为1.5NA | ||
| C. | 1mol H2O含有的水分子数目为NA | D. | 0.5NACl2分子的物质的量是0.5mol |
20.下列实验操作对应的图象不正确的是( )
| 选项 | A | B | C | D |
| 实验操作 | 向MgCl2、AlCl3溶液中(各1mol),逐滴加入NaOH溶液 | 向HCl、MgCl2、AlCl3、NH4Cl溶液中(各1mol),逐滴加入NaOH溶液 | 向NaOH、NaAlO2溶液中(各1mol),逐滴加入HCl溶液 | 向NaOH、Na2CO3混合溶液中(各1mol)滴加稀盐酸 |
| 图象 |  |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
7.利用下列装置,可完成很多电化学实验.下列有关叙述,正确的是( )


| A. | 若X为锌棒,开关K置于A处,可减缓铁的腐蚀,这种方法称为牺牲阴极的阳极保护法 | |
| B. | 若X为铜棒,开关K置于A处,装置中发生的总反应为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑ | |
| C. | 若X为碳棒,开关K置于B处,向食盐水中滴入酚酞溶液可看到碳棒附近先变红 | |
| D. | 若X为碳棒,开关K置于B处,在铁棒附近滴入硫氰化钾溶液可看到溶液变血红色 |
4.下列溶液中Cl-浓度最大的是( )
| A. | 200mL 2mol/L MgCl2溶液 | |
| B. | 1000mL 2.5mol/L NaCl溶液 | |
| C. | 10g AgCl固体加入 300mL水充分搅拌 | |
| D. | 250mL 1mol/L AlCl3溶液 |
 )是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线:
)是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线: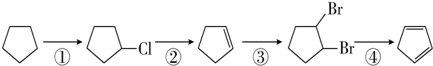
 ),途径如下:
),途径如下: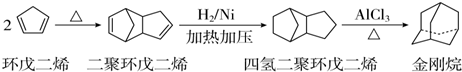
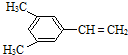 、
、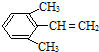 .
.