题目内容
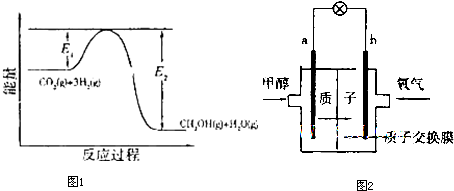
某反应△H=+100kJ?mol-1,下列有关该反应的叙述正确的是( )
| A、正反应活化能小于100kJ?mol-1 |
| B、逆反应活化能一定小于100kJ?mol-1 |
| C、逆反应活化能大于正反应活化能 |
| D、正反应活化能不小于100kJ?mol-1 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:某反应△H=+100kJ?mol-1,应为吸热反应,说明反应物总能量小于生成物总能量,结合焓变与活化能的关系是△H=正反应的活化能-逆反应的活化能判断.
解答:
解:某反应的△H=-100kJ?mol-1,则正反应的活化能-逆反应的活化能=+100kJ?mol-1,说明正反应的活化能比逆反应的活化能大100kJ?mol-1,无法确定正、逆反应活化能的大小,只有D正确.
故选D.
故选D.
点评:本题考查了反应能量变化和焓变、活化能的含义理解,为高频考点,侧重学生的分析能量和基本概念的综合理解和运用的考查,注意把握反应的实质,题目难中等.

练习册系列答案
相关题目
下列溶液显酸性的是( )
| A、NaCl溶液 |
| B、Na2CO3溶液 |
| C、AlCl3溶液 |
| D、KNO3溶液 |
我国城市环境污染的大气污染物主要是( )
| A、CO2、Cl2、N2、酸雨 |
| B、SO2、NO2、CO、烟尘 |
| C、NH3、CO2、NO2、雾 |
| D、HCl、SO2、N2、粉尘 |
依据元素周期表及元素周期律,下列推断正确的是( )
| A、含有离子键和共价键的化合物一定是离子化合物 |
| B、元素原子的最外层电子数等于该元素的最高化合价 |
| C、由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| D、VIIA族元素阴离子的还原性越强,元素最高价氧化物对应水化物的酸性也越强 |
下列分子立体构型是平面正三角是( )
| A、H2S |
| B、NH3 |
| C、SO3 |
| D、CS2 |
某元素一个原子的质量为ag,一个C-12原子的质量为bg,则该元素的相对原子质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列各组中的离子能在溶液中大量共存的是( )
| A、H+Ca2+ Cl-CO32- |
| B、Na+ Mg2+SO42- OH- |
| C、K+ Na+ OH- Cl- |
| D、Cu2+ Ba2+ Cl- SO42- |