题目内容
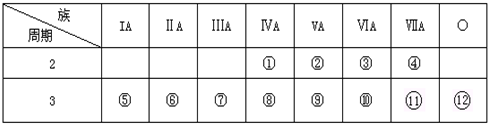
1.如图为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述中不正确的是( )
| A. | A、C两元素形成的化合物都为共价化合物 | |
| B. | AD2的电子式为 | |
| C. | B、C形成的化合物BC中所含化学键为非极性共价键 | |
| D. | B2的结构式为N≡N |
分析 由短周期元素的位置可知,A为碳、B为氮、C为氧、D为S.
A.碳元素与氧元素形成CO、CO2,均为共价化合物;
B.CS2与CO2的结构相似;
C.NO中N原子、O原子对共用电子对吸引能力不同,共用电子对偏向氧原子;
D.N2分子中N原子之间形成3对共用电子对.
解答 解:由短周期元素的位置可知,A为碳、B为氮、C为氧、D为S.
A.碳元素与氧元素形成CO、CO2,均为共价化合物,故A正确;
B.CS2与CO2的结构相似,分子中C原子与S原子之间形成2对共用电子对,电子式为 ,故B正确;
,故B正确;
C.NO中N原子、O原子对共用电子对吸引能力不同,共用电子对偏向氧原子,所含化学键为极性共价键,故C错误;
D.N2分子中N原子之间形成3对共用电子对,其结构式为N≡N,故D正确,
故选:C.
点评 本题考查元素周期表、电子式、化学键等,比较基础,有利于基础知识的巩固.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
20.有关如图及实验的描述正确的是( )
| A. |  用图装置蒸发FeCl3溶液制备无水FeCl3 用图装置蒸发FeCl3溶液制备无水FeCl3 | |
| B. |  用图装置电解精炼铝 用图装置电解精炼铝 | |
| C. |  用图装置构成铜锌原电池 用图装置构成铜锌原电池 | |
| D. |  用图装置定量测定化学反应速率 用图装置定量测定化学反应速率 |
1. 甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是:
甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是:
CH4(g)+H2O(g)=CO(g)+3H2(g)
其他条件相同,在不同催化剂(Ⅰ、Ⅱ)作用下反应相同时间后,体系中CO含量随反应温度的变化如图所示.下列说法正确的是( )
 甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是:
甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是:CH4(g)+H2O(g)=CO(g)+3H2(g)
其他条件相同,在不同催化剂(Ⅰ、Ⅱ)作用下反应相同时间后,体系中CO含量随反应温度的变化如图所示.下列说法正确的是( )
| A. | 相同条件下,催化剂Ⅱ催化效率更高 | |
| B. | b点表示上述反应在对应条件下的平衡状态 | |
| C. | 根据图象,无法判断该反应是否为吸热反应 | |
| D. | 该反应平衡常数表达式为K=$\frac{c(CO)•c3(H2)}{c(CH4)}$ |
9.下列说法正确的是( )
| A. | 章鱼胺的结构为 ,其分子式为C8H12NO2 ,其分子式为C8H12NO2 | |
| B. | 鸡蛋白可溶于水,加浓硫酸钠溶液和福尔马林均可使鸡蛋白溶液聚沉,但原理不同 | |
| C. | 葡萄糖、蔗糖、淀粉都属于糖类,三者互为同系物 | |
| D. |  与足量H2反应的产物为3-甲基-2-乙基戊烷 与足量H2反应的产物为3-甲基-2-乙基戊烷 |
6.下列各组混合物中,不论二者以什么比例混合,只要总质量一定,完全燃烧时生成CO2的质量也一定,不符合上述要求的是( )
| A. | 苯、甲苯 | B. | 乙炔、苯乙烯 | C. | 甲醛、甲酸甲酯 | D. | 乙烯、环己烷 |
13.向 Cr2 (SO4)3 的水溶液中加入NaOH溶液,当pH=4.6时开始出现Cr(OH)3沉淀,随着pH的升高,沉淀增多,当pH≥13时,沉淀消失,出现亚铬酸根离子(CrO2-),其平衡关系:
Cr3++3OH-?Cr(OH)3?CrO2-+H++H2O
(紫色) (灰绿色) (亮绿色)
向50mL 0.05mol•L-1的Cr2(SO4)3 溶液中加入等体积1.0mol•L-1的 NaOH溶液,充分反应后,溶液中可观察到的现象为( )
Cr3++3OH-?Cr(OH)3?CrO2-+H++H2O
(紫色) (灰绿色) (亮绿色)
向50mL 0.05mol•L-1的Cr2(SO4)3 溶液中加入等体积1.0mol•L-1的 NaOH溶液,充分反应后,溶液中可观察到的现象为( )
| A. | 溶液为紫色 | B. | 溶液为亮绿色 | ||
| C. | 溶液中有灰绿色沉淀 | D. | 无法判断 |
10.下列有机物系统命名正确的是( )
| A. |  | B. |  | C. |  | D. | 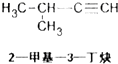 |
11.下列说法正确的是( )
| A. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| B. | 同温同压下,H2 (g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 已知:①2H2(g)+O2(g)═2H2O(g)△H=-a kJ•mol-1,②2H2(g)+O2 (g)═2H2O(1)△H=-b kJ•mol-1,则a>b | |
| D. | 已知:①C(s,石墨)+O2 (g)═CO2(g)△H=-393.5 kJ•mol-1,②C(s,金刚石)+O2(g)═CO2 (g)△H=-395.0 kJ•mol-1,则C(s,石墨)═C(s,金刚石)△H=+1.5 kJ•mol-1 |