题目内容
下列说法正确的是( )
| A、直接加热蒸干FeCl3溶液,可得FeCl3固体 |
| B、加入催化剂可加快反应速率,并提高反应物的转化率 |
| C、pH值相同的CH3COOH溶液和NH4Cl溶液中,水的电离程度相同 |
| D、可用Na2CO3溶液处理水垢中的CaSO4,转化为易于除去的CaCO3 |
考点:盐类水解的应用,化学反应速率的影响因素,弱电解质在水溶液中的电离平衡,难溶电解质的溶解平衡及沉淀转化的本质
专题:基本概念与基本理论
分析:A、FeCl3能水解生成Fe(OH)3和HCl;
B、催化剂对平衡无影响;
C、酸抑制水的电离,易水解的盐促进水电离;
D、根据沉淀转化原理分析.
B、催化剂对平衡无影响;
C、酸抑制水的电离,易水解的盐促进水电离;
D、根据沉淀转化原理分析.
解答:
解:A、FeCl3能水解生成Fe(OH)3和HCl,加热HCl挥发,促进水解,所以得不到FeCl3固体,故A错误;
B、催化剂能增大反应速率,但是对平衡无影响,所以转化率不变,故B错误;
C、酸抑制水的电离,易水解的盐促进水电离,所以pH值相同的CH3COOH溶液和NH4Cl溶液中,水的电离程度后者大,故C错误;
D、碳酸钙的溶解度比硫酸钙的小,所以CaSO4中加Na2CO3溶液会转化为碳酸钙沉淀,故D正确;
故选D.
B、催化剂能增大反应速率,但是对平衡无影响,所以转化率不变,故B错误;
C、酸抑制水的电离,易水解的盐促进水电离,所以pH值相同的CH3COOH溶液和NH4Cl溶液中,水的电离程度后者大,故C错误;
D、碳酸钙的溶解度比硫酸钙的小,所以CaSO4中加Na2CO3溶液会转化为碳酸钙沉淀,故D正确;
故选D.
点评:本题考查了盐的水解,催化剂对速率和平衡的影响,影响水的电离的因素,沉淀的转化,属于基本原理的应用方面的考查,题目难度不大.

练习册系列答案
相关题目
邻甲基苯甲酸(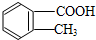 )有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )
)有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )
 )有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )
)有多种同分异构体,其中属于酯类的含有苯环的同分异构体有( )| A、6种 | B、2种 | C、4种 | D、5种 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是( )
| A、每生成1mol Na2Mn5O10转移2mol电子 |
| B、AgCl是还原产物 |
| C、Na+不断向“水”电池的负极移动 |
| D、正极反应式:Ag+Cl--e-=AgCl |
 控制适宜条件,将反应Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s)△H<0,设计成如图所示的原电池,一段时间后,灵敏电流计读数为零.则下列判断不正确的是( )
控制适宜条件,将反应Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s)△H<0,设计成如图所示的原电池,一段时间后,灵敏电流计读数为零.则下列判断不正确的是( )| A、此时化学反应达到平衡状态 |
| B、若此时将Sn电极换成质量较大的Sn 电极后,电流计指针偏转,c(Pb2+)将减小 |
| C、若此时向左池加入少量的Sn(NO3)2固体,电流计指针偏转,Sn电极为正极 |
| D、若此时升高温度,c(Sn2+)将减小,Pb电极为负极 |
分子式为C8H10的芳香烃,其一氯代物不可能有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
“酸化”是实验中经常采用的方法,下列酸化过程正确的是( )
| A、提高高锰酸钾的氧化能力,用盐酸酸化 |
| B、抑制Fe2+的水解,用稀硝酸酸化 |
| C、检验氯代烃中含氯,加碱溶液加热后,用硫酸酸化,再检验 |
| D、确认溶液中含有SO42-时,用盐酸酸化,再检验 |
下列说法不正确的是( )
| A、室温下,pH=2的酸溶液与pH=12的强碱溶液等体积混合,所得溶液pH≤7 |
| B、某溶液中加入稀盐酸产生无色气体,将该气体通入澄清石灰水中变混浊,原溶液中一定含有大量CO32-或SO32- |
| C、某试液中加入盐酸酸化的氯化钡溶液,有白色沉淀,该溶液中一定含有SO42- |
| D、0.1mol/L弱酸HA溶液与 0.05mol/LNaOH溶液等体积混合后,所得溶液微粒浓度是2c(H+)+c(HA)=c(A-)+2c(OH-) |
 室温下,将0.1mol?L-1盐酸滴入20mL 0.1mol?L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.
室温下,将0.1mol?L-1盐酸滴入20mL 0.1mol?L-1氨水中,溶液pH随加入盐酸体积的变化曲线如图所示.