题目内容
已知A、B、C、D均为短周期元素,它们的原子序数依次递增. A是最外层为一个电子的非金属元素,C 原子的最外层电子数是次外层的3倍; C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物.A、B、C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为A:B:C=4:2:3.请回答下列问题:
(1)写出B的原子结构示意图 ,写出C和D形成的淡黄色固体化合物的电子式 .
(2)元素原子的物质的量之比为A:B:C=4:2:3 的晶体名称为 ,其水溶液显 性,其反应的离子方程式为 .
(3)请写出A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两种元素组成的微粒的符号(举两例) 、 .
(4)写出由B、C元素组成且元素原子质量比为B:C=7:12的化合物的化学式 .
(1)写出B的原子结构示意图
(2)元素原子的物质的量之比为A:B:C=4:2:3 的晶体名称为
(3)请写出A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两种元素组成的微粒的符号(举两例)
(4)写出由B、C元素组成且元素原子质量比为B:C=7:12的化合物的化学式
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D均为短周期元素,它们的原子序数依次递增,A是最外层为一个电子的非金属元素,则A为氢元素,C 原子的最外层电子数是次外层的3倍,则C为氧元素; C和D可形成两种固态化合物,其中一种为淡黄色固体,则D为钠元素;B和C可形成多种气态化合物,说明B、C都为非金属元素,A、B、C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为A:B:C=4:2:3,则该晶体为NH4NO3,所以B为氮元素,据此答题;
解答:
解:A、B、C、D均为短周期元素,它们的原子序数依次递增,A是最外层为一个电子的非金属元素,则A为氢元素,C 原子的最外层电子数是次外层的3倍,则C为氧元素; C和D可形成两种固态化合物,其中一种为淡黄色固体,则D为钠元素;B和C可形成多种气态化合物,说明B、C都为非金属元素,A、B、C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为A:B:C=4:2:3,则该晶体为NH4NO3,所以B为氮元素,
(1)由上面的分析可知,B为氮元素,它的原子结构示意图为 ,C和D形成的淡黄色固体化合物为过氧化钠,它的电子式为
,C和D形成的淡黄色固体化合物为过氧化钠,它的电子式为 ,
,
故答案为: ;
; ;
;
(2)元素原子的物质的量之比为H:N:O=4:2:3 的晶体名称为硝酸铵,因为铵根离子水解,所以其水溶液显酸性,其反应的离子方程式为NH4++H2O?NH3?H2O+H+,
故答案为:硝酸铵;酸;NH4++H2O?NH3?H2O+H+;
(3)与H2O和NH3分子中电子数相同,且仍由H、N、O元素中任意两种元素组成的微粒有NH4+,NH2-,OH-,H3O+等,
故答案为:NH4+,NH2-,OH-,H3O+等;
(4)由N、O元素质量比为7:12的化合物中,N、O原子个数比为
:
=2:3,所以该化合物的化学式为N2O3,
故答案为:N2O3;
(1)由上面的分析可知,B为氮元素,它的原子结构示意图为
 ,C和D形成的淡黄色固体化合物为过氧化钠,它的电子式为
,C和D形成的淡黄色固体化合物为过氧化钠,它的电子式为 ,
,故答案为:
 ;
; ;
;(2)元素原子的物质的量之比为H:N:O=4:2:3 的晶体名称为硝酸铵,因为铵根离子水解,所以其水溶液显酸性,其反应的离子方程式为NH4++H2O?NH3?H2O+H+,
故答案为:硝酸铵;酸;NH4++H2O?NH3?H2O+H+;
(3)与H2O和NH3分子中电子数相同,且仍由H、N、O元素中任意两种元素组成的微粒有NH4+,NH2-,OH-,H3O+等,
故答案为:NH4+,NH2-,OH-,H3O+等;
(4)由N、O元素质量比为7:12的化合物中,N、O原子个数比为
| 7 |
| 14 |
| 12 |
| 16 |
故答案为:N2O3;
点评:本题主要考查了原子结构示意图、盐类的水解、化学式的计算等知识点,难度不大,解题时注意根据元素原子结构和元素的性质确定元素种类.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列物质的水溶液能够导电,但属于非电解质的是( )
| A、H2S |
| B、碳酸氢钠 |
| C、氨气 |
| D、氢氧化钾 |
下列关于能量转换的认识中,不正确的是( )
| A、电解水生成氢气和氧气时,电能转化为化学能 |
| B、绿色植物进行光合作用时,太阳能转化为化学能 |
| C、每个化学反应都伴随着能量的变化 |
| D、当反应物浓度等于生成物浓度时,可逆反应一定已达到化学平衡状态 |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、常温常压下,23g的NO2含有的氧原子数为NA |
| B、已知某种元素的一种原子的质量为ag,则该元素的相对原子质量近似为aNA |
| C、某密闭容器盛有0.1molN2和0.4molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
| D、80gNH4NO3晶体中含有NH4+小于NA个 |
某反应过程能量变化如图所示,下列说法正确的是( )
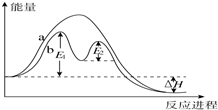

| A、反应过程a有催化剂参与 |
| B、该反应为放热反应,热效应不等于△H |
| C、使用催化剂,可改变该反应的活化能 |
| D、有催化剂条件下,反应的活化能等于E1-E2 |
向10mL 1.5mol/L的硫酸铝溶液加入30mL NaOH溶液,充分反应后得到1.56g沉淀,则NaOH溶液的物质的量浓度是( )
| A、1mol/L |
| B、2mol/L |
| C、5mol/L |
| D、3.3mol/L |

