题目内容
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、常温常压下,23g的NO2含有的氧原子数为NA |
| B、已知某种元素的一种原子的质量为ag,则该元素的相对原子质量近似为aNA |
| C、某密闭容器盛有0.1molN2和0.4molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
| D、80gNH4NO3晶体中含有NH4+小于NA个 |
考点:阿伏加德罗常数
专题:
分析:A、根据二氧化氮的物质的量求出含有的氧原子数;
B、根据元素的相对原子质量与原子的相对原子质量之间的关系判断;
C、工业上合成氨是可逆反应,不可能完全转化;
D、根据NH4NO3的物质的量求出含有的NH4+个数.
B、根据元素的相对原子质量与原子的相对原子质量之间的关系判断;
C、工业上合成氨是可逆反应,不可能完全转化;
D、根据NH4NO3的物质的量求出含有的NH4+个数.
解答:
解:A、23g二氧化氮的物质的量为0.5mol,而1molNO2含2mol氧原子,故0.5mol二氧化氮含1mol氧原子,故A正确;
B、某种元素的一种原子的质量为ag,则该原子的相对原子质量近似为aNA,该元素的相对原子质量需要根据该元素的各同位素的原子量及百分含量计算,故B错误;
C、工业上合成氨是可逆反应,0.1mol N2和0.3mol H2在某密闭容器中充分反应,不可能完全,转移电子的数目小于0.6NA,故C错误;
D、80gNH4NO3的物质的量为1mol,含有的NH4+的物质的量为1mol,个数为NA个,故D错误.
故选A.
B、某种元素的一种原子的质量为ag,则该原子的相对原子质量近似为aNA,该元素的相对原子质量需要根据该元素的各同位素的原子量及百分含量计算,故B错误;
C、工业上合成氨是可逆反应,0.1mol N2和0.3mol H2在某密闭容器中充分反应,不可能完全,转移电子的数目小于0.6NA,故C错误;
D、80gNH4NO3的物质的量为1mol,含有的NH4+的物质的量为1mol,个数为NA个,故D错误.
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是( )
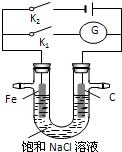

| A、K1闭合,铁棒上发生的反应为2H++2e-→H2↑ |
| B、K1闭合,石墨棒周围溶液pH逐渐升高 |
| C、K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D、K2闭合,电路中通过0.4NA个电子时,两极共产生标况下4.48L气体 |
下列说法正确的是( )
| A、标准状况下,1mol H2O和1mol H2的体积都约为22.4L |
| B、1molNa2CO3 中Na+ 的物质的量为1mol |
| C、1mol某气体的体积为22.4L |
| D、标准状况下,1g H2和 11.2LO2的物质的量相等 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、7.8g 由Na2S和Na2O2组成的混合物中含有阴离子的数目为 0.1NA |
| B、0.1molAlCl3完全转化为胶体,生成胶体粒子的数目0.l NA个 |
| C、标准状况下,22.4 L乙醇中含有分子的数目为NA |
| D、在过氧化钠与水的反应中,每生成0.1mol 氧气,转移电子的数目为0.4 NA |
下列每组反应一定能用同一离子方程式表示的是( )
| A、CaCO3、Na2CO3分别与盐酸反应 |
| B、CuO分别与稀硫酸、稀盐酸、稀硝酸反应 |
| C、H2SO4、K2SO4溶液分别与Ba(OH)2溶液反应 |
| D、Na分别与水、稀盐酸反应 |