题目内容
19.下列对乙烯分子的叙述中错误的是( )| A. | 乙烯分子里所有的原子在同一平面上 | |
| B. | 乙烯的结构简式为CH2CH2,电子式为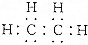 | |
| C. | 乙烯分子中碳氢键之间的夹角约为120° | |
| D. | 乙烯分子中既含有极性键又含有非极性键 |
分析 A.乙烯为平面结构;
B.烯烃分子中碳原子之间形成2对共用电子对,结构简式中碳碳双键不能省略;
C.乙烯为平面结构,碳氢键之间的夹角约为120°;
D.同种元素原子之间形成非极性键,不同元素原子之间形成极性键.
解答 解:A.乙烯为平面结构,所有原子处于同一平面上,故A正确;
B.烯烃分子中碳原子之间形成2对共用电子对,电子式为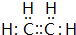 ,其结构简式为CH2=CH2,故B错误;
,其结构简式为CH2=CH2,故B错误;
C.乙烯为平面结构,碳氢键之间的夹角约为120°,故C正确;
D.乙烯分子中碳原子之间形成非极性键,C原子与H原子之间形成极性键,故D正确,
故选B.
点评 本题考查乙烯的结构、共价键类型等,比较基础,有利于基础知识的巩固.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
10.下列实验操作或事故处理中,正确的做法是( )
| A. | 氢气中混有一定量的氧气,可通过灼热的铜网来除去氧气 | |
| B. | 用无水硫酸铜检验CO2气体中是否含有水蒸气 | |
| C. | 除去SO2气体中的CO2,将混合气体通过澄清的石灰水 | |
| D. | 工业上将氯气通入澄清石灰水水制漂白粉 |
7.在加热情况下能和浓H2SO4反应放出刺激性气味气体,并将气体通入水中呈酸性,通入溴水或酸性KMnO4溶液中,颜色都消失的物质是( )
| A. | 氧化亚铁 | B. | 二氧化锰 | C. | 氧化铜 | D. | 木炭粉 |
4.下列实验操作正确的是( )
| 选项 | 实验 | 操作 |
| A | 验证Cl2和Br2的非金属性强弱 | 将少量氯水加入盛有FeBr2溶液的试管中,用力振荡后加入少量乙醇,振荡,静置 |
| B | 检验溶液中是否含有SO42- | 用HNO3溶液酸化后再加BaCl2溶液 |
| C | 证明浓硫酸有脱水性和强氧化性 | 将浓硫酸滴到蔗糖表面 |
| D | 制取Fe(OH)3胶体 | 将烧碱溶液滴加到FeCl2溶液中 |
| A. | A | B. | B | C. | C | D. | D |
6.多原子分子氰(CN)2、硫氰(SCN)2和(OCN)2的性质与卤素单质相似,故称它们为拟卤素.它们可以生成酸和盐(见下表,表中X代表F、Cl、Br或I).
(1)在表中①②③空格处应分别填写氧氰、HSCN、NaOCN.
(2)完成下列反应的化学方程式或离子方程式.
①H++SCN-+MnO2$\stackrel{△}{→}$4H++2SCN-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++(SCN)2↑+2H2O.
②(CN)2和KOH溶液反应的化学方程式为(CN)2+2KOH═KCN+KCNO+H2O
③已知阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.试写出在NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式:(CN)2+2SCN-═2CN-+(SCN)2.
| 卤素 | 氰 | 硫氰 | ① | |
| “单质” | X2 | (CN)2 | (SCN)2 | (OCN)2 |
| 酸 | HX | HCN | ② | HOCN |
| 盐 | KX | KCN | KSCN | ③ |
(2)完成下列反应的化学方程式或离子方程式.
①H++SCN-+MnO2$\stackrel{△}{→}$4H++2SCN-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++(SCN)2↑+2H2O.
②(CN)2和KOH溶液反应的化学方程式为(CN)2+2KOH═KCN+KCNO+H2O
③已知阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.试写出在NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式:(CN)2+2SCN-═2CN-+(SCN)2.
3.某氮的氧化物是大气污染物之一,在一定温度和有催化剂的条件下,该氧化物与氨气反应只生成氮气和水,若生成的氮气和水的物质的量之比为5:6,该氧化物的化学式为( )
| A. | N2O5 | B. | NO | C. | NO2 | D. | N2O3 |
4.下列指定反应的离子方程式正确的是( )
| A. | 向漂白粉溶液中通入过量的SO2气体:ClO-+SO2+H2O═HSO3-+HClO | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 向Fe(NO3) 3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |