题目内容
10.下列实验操作或事故处理中,正确的做法是( )| A. | 氢气中混有一定量的氧气,可通过灼热的铜网来除去氧气 | |
| B. | 用无水硫酸铜检验CO2气体中是否含有水蒸气 | |
| C. | 除去SO2气体中的CO2,将混合气体通过澄清的石灰水 | |
| D. | 工业上将氯气通入澄清石灰水水制漂白粉 |
分析 A.氢气不纯加热易发生爆炸;
B.白色的无水硫酸铜粉末遇水变成蓝色;
C.SO2和CO2均可使澄清石灰水变浑浊;
D.工业上通常用石灰乳与氯气反应制取漂白粉.
解答 解:A.氢气不纯加热易发生爆炸,则不能除杂,故A错误;
B.白色的无水硫酸铜粉末遇水变成蓝色,可检验,故B正确;
C.SO2和CO2均可使澄清石灰水变浑浊,将二氧化硫除掉,故C错误;
D.因为澄清石灰水中氢氧化钙浓度太低成本较高,工业上通常用石灰乳与氯气反应制取漂白粉,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离、提纯及除杂等,侧重混合物分离方法及物质性质的考查,注意实验方案的评价性、合理性、操作性及可行性考查,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
20.分别将1g Na2CO3和1g NaHCO3装在两支试管中,各加入10mL水,振荡使它们溶解,冷却到室温后,分别向两支试管中滴入2滴酚酞.下列说法正确的是( )
| A. | 两支试管中的溶液都显红色,且Na2CO3溶液比NaHCO3溶液更红 | |
| B. | 两支试管中的溶液都显红色,且两者颜色没有区别 | |
| C. | 两支试管中的溶液都显蓝色,且Na2CO3溶液比NaHCO3溶液更蓝 | |
| D. | 两支试管中的溶液都不显颜色 |
1.设NA表示阿伏伽德罗常数的值,下列有关说法正确的是( )
| A. | 标准状况下,2.24L甲醇中含有的原子总数为0.6NA | |
| B. | 室温下,500mL pH=1的稀硫酸中含有的H+总数约为0.05NA | |
| C. | 7.8g Na2O2晶体中含有的离子总数为0.4NA | |
| D. | 电解精炼铜时,若阴极得到电子总数为2NA,则阳极质量减少64g |
18.下列各组离子能大量共存的是( )
| A. | Ba2+、Fe3+、OH-、Cl- | B. | Mg2+、Na+、Cl-、SO42- | ||
| C. | NH4+、Ba2+、NO3-、OH- | D. | H+、K+、NO3-、CO32- |
5.电子计算器中所用的纽扣电池为银锌电池,其电极分别为Ag2O 和Zn,电解质溶液为KOH溶液.电极反应式为:Zn+2OH--2e-═Zn(OH)2、Ag2O+H2O+2e-═2Ag+2OH-下列叙述中,正确的是( )
| A. | 电流由锌经外电路流向氧化银 | |
| B. | 锌是负极,氧化银是正极 | |
| C. | 工作时,负极区溶液pH减小,正极区pH增大 | |
| D. | 溶液中OH-向正极移动,K+、H+向负极移动 |
15.氯仿 (CHCl3)不溶于水,密度比水大,是一种良好的有机溶剂,若保存不当受到光照射时,易被氧化而产生剧毒光气(COCl2),同时生成HCl,下列有关氯仿变质的检验正确的是( )
| A. | 用蒸馏水检验氯仿是否变质 | |
| B. | 用硝酸银溶液检验氯仿是否变质 | |
| C. | 用氢氧化钠检验氯仿是否变质 | |
| D. | 用干燥的蓝色石蕊试纸检验氯仿是否变质 |
2.从下列叙述中,可以肯定金属A比金属B的活泼性强的是( )
| A. | A,B用导线连接后浸入电解质溶液,结果电子从B流向A | |
| B. | A从酸中置换出H2比B从酸中置换H2难 | |
| C. | 1 mol A从酸中置换出H十生成的H2比1mol B从酸中置换出H十生成的H2多 | |
| D. | 常温时,A能从水中置换出氢气,而B不能 |
19.下列对乙烯分子的叙述中错误的是( )
| A. | 乙烯分子里所有的原子在同一平面上 | |
| B. | 乙烯的结构简式为CH2CH2,电子式为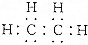 | |
| C. | 乙烯分子中碳氢键之间的夹角约为120° | |
| D. | 乙烯分子中既含有极性键又含有非极性键 |
15.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 1 molAl3+含有的核外电子数为3NA | |
| B. | 将58.5g NaCl溶于1.00 L水中,所得NaCL溶液的浓度为1.00mol•L-1 | |
| C. | 1 molCl2与足量的铁反应,转移的电子为数3Na | |
| D. | 常温下,10LpH=1的硫酸溶液中含有的H+离子数为NA. |