题目内容
18.根据下表信息,判断以下叙述正确的是( )| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点:H2T<H2R | B. | M与T形成的化合物具有两性 | ||
| C. | 单质与稀盐酸反应的速率:L<Q | D. | L2+与R2-的核外电子数相等 |
分析 短周期元素中,R、T都有-2价,应位于周期表第ⅥA族,其中R有+6价,则T为O元素,R为S元素;L、Q都有+2价,处于ⅡA族,且L的原子半径较大,则L为Mg,Q为Be;M最高正价为+3价,原子半径介于Mg、S之间,可确定M为Al,据此解答.
解答 解:短周期元素中,R、T都有-2价,应位于周期表第ⅥA族,其中R有+6价,则T为O元素,R为S元素;L、Q都有+2价,处于ⅡA族,且L的原子半径较大,则L为Mg,Q为Be;M最高正价为+3价,原子半径介于Mg、S之间,可确定M为Al.
A.由于水分子之间存在氢键,故沸点H2O>H2S,即H2T>H2R,故A错误;
B.M与T形成的化合物是氧化铝,属于两性氧化物,故B正确;
C.金属性Mg比Be强,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为L>Q,故C错误;
D.Mg2+离子核外电子数为10,S2-离子的核外电子数为18,二者核外电子数不相等,故D错误,
故选B.
点评 本题考查性质结构位置关系应用,难度中等,根据元素化合价与半径确定元素是解题关键,注意基础知识的全面掌握.

练习册系列答案
相关题目
8.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA | |
| B. | 1.8g重水(D2O)中含有的质子数和电子数均为1.0NA | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA | |
| D. | 常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
10.一种无色气体100mL,由NH3、NO、CO2所组成,将此无色气体通过浓硫酸的洗气瓶后,发现气体减少了30mL.剩余气体继续通过Na2O2固体后,发现气体变成红棕色,再将该气体通入盛满水倒立于水槽中的试管内,发现试管内水位上升,最后试管内充满液体.则原混合气体中NH3、NO、CO2气体的体积比为( )
| A. | 5:8:12 | B. | 15:14:21 | C. | 10:14:21 | D. | 30:28:23 |
8.活性炭可处理大气污染物NO.T℃时,在容积为2L的密闭容器中加入NO和一定量的炭粉在一定条件下发生如下可逆反应:C(s)+2NO(g)?CO2(g)+N2(g),测得各物质的物质的量如下表:
(1)一定温度下,在体积恒定的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是a、d(填字母序号).
a.单位时间内生成2mol NO,同时生成1mol N2
b.NO物质的量与CO2物质的量之比为2:1
c.容器中混合气体的压强不变
d.混合气体的密度不变
(2)0~2min内,用NO表示该反应的平均速率υ(NO)=0.1mol?L-1?min-1.
(3)已知升高温度,该可逆反应的化学平衡常数K增大,则该反应是吸热反应(填“吸热”或“放热”).T℃时,该反应的化学平衡常数K=9/16,则2min时正反应速率大于(填“大于”、“等于”或“小于”)逆反应速率.当该反应达到平衡时,NO的平衡转化率为60.0%.
(4)若其他条件不变,改变下列条件后,所得结论正确的是a、b(填字母序号).
a.恒压时,向容器中充入氦气,反应速率减小
b.升高温度,化学平衡正向移动
c.增大NO的浓度,NO的转化率增大
d.缩小容器的体积,平衡常数增大.
| 活性炭(mol) | NO(mol) | CO2(mol) | N2(mol) | |
| 起始状态 | 3.0 | 0.8 | 0 | 0 |
| 2min时 | 2.8 | 0.4 | 0.2 | 0.2 |
a.单位时间内生成2mol NO,同时生成1mol N2
b.NO物质的量与CO2物质的量之比为2:1
c.容器中混合气体的压强不变
d.混合气体的密度不变
(2)0~2min内,用NO表示该反应的平均速率υ(NO)=0.1mol?L-1?min-1.
(3)已知升高温度,该可逆反应的化学平衡常数K增大,则该反应是吸热反应(填“吸热”或“放热”).T℃时,该反应的化学平衡常数K=9/16,则2min时正反应速率大于(填“大于”、“等于”或“小于”)逆反应速率.当该反应达到平衡时,NO的平衡转化率为60.0%.
(4)若其他条件不变,改变下列条件后,所得结论正确的是a、b(填字母序号).
a.恒压时,向容器中充入氦气,反应速率减小
b.升高温度,化学平衡正向移动
c.增大NO的浓度,NO的转化率增大
d.缩小容器的体积,平衡常数增大.

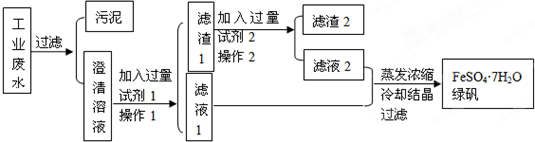
 .另外尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.请回答下列问题:
.另外尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3.请回答下列问题:
 硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途.回答下列问题:
硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途.回答下列问题: ;
;