��Ŀ����
13��W��X��Y��Z�������ڱ���ǰ18��Ԫ�أ���֪����1��W�������Ӻ�Y�������Ӿ�����ͬ�ĺ�������Ų��������γ����ΪWY�Ļ����
��2��Y��Z��ͬ��Ԫ�أ��������γ����ֳ��������
��3��X��Y����ͬһ���ڣ������γɵĻ�����ȿ������ᷴӦ�ֿ�����ǿ�Ӧ��
��4��Y����������������Ӳ�����������
��ش�
��1��WԪ���ǣ�Mg��ZԪ����S��
��2��������WY�Ļ�ѧʽ��MgO��
��3��Y��Z�γ����ֳ���������ķ���ʽ��SO2��SO3��
��4��д��X��Y�γɵĻ�������NaOH��Һ��Ӧ�ķ���ʽAl2O3+2OH-=AlO2-+2H2O��
���� Y����������������Ӳ�������������Yֻ�ܴ��ڵڶ����ڣ�����������Ϊ6��ΪOԪ�أ�
X��Y����ͬһ���ڣ������γɵĻ�����ȿ������ᷴӦ�ֿ�����ǿ�Ӧ���û�����Ϊ����������XΪAlԪ�أ�
Y��Z��ͬ��Ԫ�أ��������γ����ֳ����������ZΪSԪ�أ�
W��������Y�������Ӿ�����ͬ�ĺ�������Ų��������γ����ΪWY�Ļ����YΪ�����ӣ���Wֻ��ΪMgԪ�أ��ݴ˽��н��
��� �⣺Y����������������Ӳ�������������Yֻ�ܴ��ڵڶ����ڣ�����������Ϊ6��ΪOԪ�أ�X��Y����ͬһ���ڣ������γɵĻ�����ȿ������ᷴӦ�ֿ�����ǿ�Ӧ���û�����Ϊ����������XΪAlԪ�أ�Y��Z��ͬ��Ԫ�أ��������γ����ֳ����������ZΪSԪ�أ�W��������Y�������Ӿ�����ͬ�ĺ�������Ų��������γ����ΪWY�Ļ����YΪ�����ӣ���Wֻ��ΪMgԪ�أ�
��1�����ݷ�����֪��WԪ����Mg��ZԪ����S��
�ʴ�Ϊ��Mg��S��
��2��WΪMg��YΪO������WY�Ļ�ѧʽ��MgO��
�ʴ�Ϊ��MgO��
��3��Y��Z�ֱ�ΪO��S�������γ����ֳ���������ķ���ʽ��SO2��SO3��
�ʴ�Ϊ��SO2��SO3��
��4��X��Y�γɵĻ�����Ϊ����������������NaOH��Һ��Ӧ����ƫ�����ƺ�ˮ����Ӧ�����ӷ���ʽΪ��Al2O3+2OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al2O3+2OH-=AlO2-+2H2O��
���� ���⿼����λ�á��ṹ�����ʹ�ϵ��Ӧ�ã���Ŀ�ѶȲ�����ȷ�ƶ�Ԫ��Ϊ���ؼ���ע������ԭ�ӽṹ��Ԫ�����ڱ���Ԫ�������ɵĹ�ϵ����ȷ��Ԫ�ص��ʼ��仯�������ʣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | 10��1 | B�� | 1��10 | C�� | 2��1 | D�� | 4��5 |
| ѡ�� | ���ʼ����� | ���� | �����Լ��� |
| A | I2��Cl2�� | ʪ��ĵ���-KI��ֽ | NaI��Һ |
| B | NaHCO3��Һ��Na2CO3�� | Ca��OH��2��Һ | ����CO2 |
| C | CO2��HCl�� | AgNO3��Һ����ϡ���ᣩ | ����Na2CO3��Һ |
| D | NO��NO2�� | �۲���ɫ��ʪ��ĵ���-KI��ֽ | ˮ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | 1��3 | B�� | 3��1 | C�� | 1��1 | D�� | 3��2 |
| A�� | Al | B�� | Al��OH��3 | C�� | AlCl3 | D�� | Al2O3 |
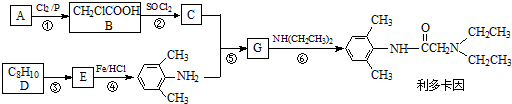
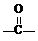 OH$\stackrel{SOCl_{2}}{��}$R
OH$\stackrel{SOCl_{2}}{��}$R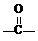 Cl
Cl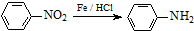
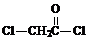 ���ķ�Ӧ������ȡ����Ӧ��
���ķ�Ӧ������ȡ����Ӧ�� ��
��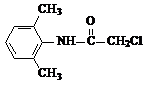 +2NaOH$\stackrel{��}{��}$
+2NaOH$\stackrel{��}{��}$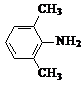 +HOCH2COONa+NaCl��
+HOCH2COONa+NaCl��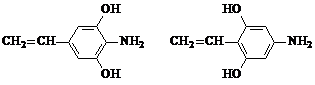 ��
��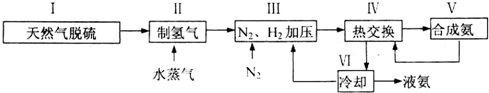
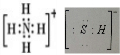 ��д��������Ӧ�Ļ�ѧ����ʽ��2NH4HS+O2$\frac{\underline{\;һ������\;}}{\;}$2NH3•H2O+2S��NH3�ķе����H2S������ΪNH3����֮�������һ�ֽз��Ӽ����õ���������
��д��������Ӧ�Ļ�ѧ����ʽ��2NH4HS+O2$\frac{\underline{\;һ������\;}}{\;}$2NH3•H2O+2S��NH3�ķе����H2S������ΪNH3����֮�������һ�ֽз��Ӽ����õ���������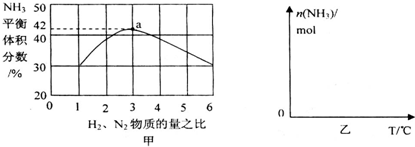
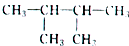 ��ϵͳ����Ϊ2��3-�������飻
��ϵͳ����Ϊ2��3-�������飻