题目内容
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的( )
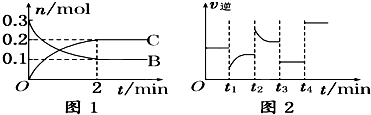

| A、反应开始2分钟内,v(B)=0.05mol/(L?min) |
| B、t1时改变的条件可能是减小了反应物的浓度 |
| C、t2时可能升高了温度 |
| D、t3时改变的条件可能是降压,此时c(B)减小 |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:A、再根据v=
计算v(B);
B、减小反应物的浓度,正逆速率都减小,并且逆反应速度降低的幅度更大,反应逆向移动,据此判断;
C、升高温度,正逆反应速率加快,据此判断;
D、降低压强会减慢反应速率,平衡不移动,据此判断.
| ||
| △t |
B、减小反应物的浓度,正逆速率都减小,并且逆反应速度降低的幅度更大,反应逆向移动,据此判断;
C、升高温度,正逆反应速率加快,据此判断;
D、降低压强会减慢反应速率,平衡不移动,据此判断.
解答:
解:A、通过图1可知,v(B)=
=0.05 mol/(L?min),故A错误;
B、减小反应物的浓度,正逆速率都减小,速率会离开原来的速率点开始减小,故B正确;
C、升高温度,正逆反应速率加快,故C错误;
D、降低压强,会减慢反应速率,但是不会影响该平衡的移动,此时c(B)不变,故D错误.
故选B.
| ||
| 2min |
B、减小反应物的浓度,正逆速率都减小,速率会离开原来的速率点开始减小,故B正确;
C、升高温度,正逆反应速率加快,故C错误;
D、降低压强,会减慢反应速率,但是不会影响该平衡的移动,此时c(B)不变,故D错误.
故选B.
点评:本题考查化学反应速率和化学平衡的图象问题,难度不大,注意图2中纵坐标是表示逆反应速率,注意条件变化逆反应速率随实际变化.

练习册系列答案
相关题目
下列物质保存方法正确的是( )
①金属钠一煤油或石蜡油; ②过氧化钠一塑料瓶密封;
③水玻璃一橡胶塞细口瓶; ④氯水一毛玻璃塞棕色细口瓶;
⑤苯一毛玻璃塞无色细口瓶; ⑥浓、稀硝酸 毛玻璃塞棕色细口瓶.
①金属钠一煤油或石蜡油; ②过氧化钠一塑料瓶密封;
③水玻璃一橡胶塞细口瓶; ④氯水一毛玻璃塞棕色细口瓶;
⑤苯一毛玻璃塞无色细口瓶; ⑥浓、稀硝酸 毛玻璃塞棕色细口瓶.
| A、全部 | B、⑤④⑥ |
| C、②④⑥ | D、①②③ |
2005年11月13日,中国石油吉林石化公司双苯厂一装置发生爆炸,导致严重污染.这次爆炸产生的主要污染物为硝基苯、苯和苯胺等.下列说法正确的是( )
| A、硝基苯是由苯与浓硝酸在浓硫酸作用下发生取代反应制取的 |
| B、苯可以发生取代反应也可以发生加成反应,但不可被氧化 |
| C、硝基苯有毒,密度比水小,可从水面上“捞出” |
| D、苯与硝基苯都属于芳香族化合物 |
用一种试剂可区分乙醇、乙醛、乙酸、甲酸,该试剂是( )
| A、酸性高锰酸钾溶液 |
| B、溴水 |
| C、氯化铁溶液 |
| D、新制氢氧化铜 |
将铁屑溶于滴有KSCN溶液的过量盐酸后,再加入下列物质,溶液呈红色的是( )
| A、硫酸 | B、氯水 |
| C、氯化钾 | D、氯化铜 |
以下说法中正确的是( )
| A、相同温度下,1 mol/L氨水溶液与0.5 mol/L氨水溶液中c(OH-) 之比为2:1 |
| B、NH4Cl 溶液中,c(NH4+)=c(Cl -) |
| C、向0.1 mol/L NaNO3溶液中滴加稀盐酸,使溶液pH=5,此时混合液中c(Na+)=c(NO3-) |
| D、向醋酸钠溶液中加入适量醋酸,使混合液的pH=7,此时混合液中c(Na+)=c(CH3COO-) |