题目内容
3.在标准状态下,下列离子中Sm⊙为0的是( )| A. | Na+ | B. | Cu2+ | C. | H+ | D. | Cl- |
分析 规定298K时1mol水合氢离子的标准摩尔熵为0kJ/mol.298K时若1mol某离子混乱度大于1mol水合氢离子,则其标准摩尔熵大于0,反之则小于0,以此来解答.
解答 解:标准状态下,下列离子中Sm⊙为0的是H+,
故选C.
点评 本题考查标准摩尔熵,把握标准状态下氢离子的摩尔熵为0为解答的关键,侧重分析与应用能力的考查,注意混乱度的判断,题目难度不大.

练习册系列答案
相关题目
13.标准状况下有三种气体:①6.72L NH3 ②1.204×1023个 H2S ③5.6g CH4,下列关系正确的是( )
| A. | 体积大小:③>②>① | B. | 原子数目:③>①>② | C. | 密度大小:②>③>① | D. | 质量大小:②>①>③ |
18.在1mol/L CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+,要使溶液pH下降,可采取( )
①加NaOH(s)②加水③加CH3COOH④加CH3COONa(s)⑤加CaCO3(s)⑥加HCl(g)
①加NaOH(s)②加水③加CH3COOH④加CH3COONa(s)⑤加CaCO3(s)⑥加HCl(g)
| A. | ①④ | B. | ③⑥ | C. | 只有② | D. | 只有⑤ |
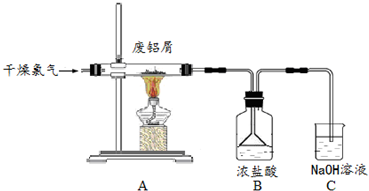
10.实验室采用简易装置模拟演示工业炼铁原理.实验装置图和实验步骤如下:
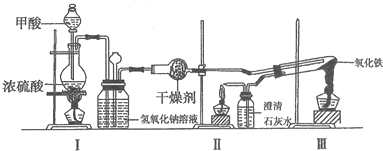
①按如图连接好装置,检查装置气密性.
②称取适量Fe2O3于石英试管中,点燃I处酒精灯,缓慢滴入甲酸.
③在完成某项操作后,点燃另外两处酒精灯.
④30min后熄灭酒精灯,关闭弹簧夹.
⑤待产物冷却至室温后,收集产物.
⑥采用如上方法分别收集带金属网罩酒精灯(金属网罩可以集中火焰、提高温度)和酒精喷灯加热的产物.请回答下列问题:
(1)制备CO的原理是利用甲酸(HCOOH)在浓硫酸加热条件下分解,盛放甲酸的仪器名称为分液漏斗,该反应的化学方程式为HCOOH $→_{△}^{浓硫酸}$CO↑+H2O.
(2)实验步骤③“某项操作”是指检验CO纯度.
(3)实验步骤④熄灭酒精灯的顺序为Ⅲ、I、II.(用“I”、“Ⅱ”、“Ⅲ”表示)
(4)通过查资料获取如下信息:
I.酒精灯平均温度为600℃;加网罩酒精灯平均温度为700℃,酒精喷灯平均温度为930℃.
Ⅱ.资料指出当反应温度高于710℃时,Fe能稳定存在,在680~710℃之间时,FeO能稳定存在,低于680℃,则主要是Fe3O4.试分析酒精灯加热条件下生成Fe的原因:长时间集中加热使局部温度达到还原生成铁所需要的温度.
(5)已知FeO、Fe2O3、Fe3O4中氧元素的质量分数分别为:22.2%、30%、27.6%.
利用仪器分析测出3种样品所含元素种类和各元素的质量分数如表:
分析各元素的质量分数可知前两种加热方式得到的产物为混合物,其中酒精灯加热所得产物的组成最多有9种可能.
(6)通过进一步的仪器分析测出前两种加热方式得到的固体粉末成分均为Fe3O4和Fe,用酒精喷灯加热得到的固体粉末成分为Fe.请计算利用酒精灯加热方式所得混合物中Fe3O4和Fe的质量比为12:1.(要求保留整数).

①按如图连接好装置,检查装置气密性.
②称取适量Fe2O3于石英试管中,点燃I处酒精灯,缓慢滴入甲酸.
③在完成某项操作后,点燃另外两处酒精灯.
④30min后熄灭酒精灯,关闭弹簧夹.
⑤待产物冷却至室温后,收集产物.
⑥采用如上方法分别收集带金属网罩酒精灯(金属网罩可以集中火焰、提高温度)和酒精喷灯加热的产物.请回答下列问题:
(1)制备CO的原理是利用甲酸(HCOOH)在浓硫酸加热条件下分解,盛放甲酸的仪器名称为分液漏斗,该反应的化学方程式为HCOOH $→_{△}^{浓硫酸}$CO↑+H2O.
(2)实验步骤③“某项操作”是指检验CO纯度.
(3)实验步骤④熄灭酒精灯的顺序为Ⅲ、I、II.(用“I”、“Ⅱ”、“Ⅲ”表示)
(4)通过查资料获取如下信息:
I.酒精灯平均温度为600℃;加网罩酒精灯平均温度为700℃,酒精喷灯平均温度为930℃.
Ⅱ.资料指出当反应温度高于710℃时,Fe能稳定存在,在680~710℃之间时,FeO能稳定存在,低于680℃,则主要是Fe3O4.试分析酒精灯加热条件下生成Fe的原因:长时间集中加热使局部温度达到还原生成铁所需要的温度.
(5)已知FeO、Fe2O3、Fe3O4中氧元素的质量分数分别为:22.2%、30%、27.6%.
利用仪器分析测出3种样品所含元素种类和各元素的质量分数如表:
| 加热方式 | 产物元素组成 | 各元素的质量分数% | |
| Fe | O | ||
| 酒精灯 | Fe和O | 74.50 | 25.50 |
| 带网罩酒精灯 | Fe和O | 76.48 | 23.52 |
| 酒精喷灯 | Fe | 100.00 | 0.00 |
(6)通过进一步的仪器分析测出前两种加热方式得到的固体粉末成分均为Fe3O4和Fe,用酒精喷灯加热得到的固体粉末成分为Fe.请计算利用酒精灯加热方式所得混合物中Fe3O4和Fe的质量比为12:1.(要求保留整数).
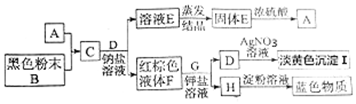
 .该反应中的氧化剂是二氧化锰.
.该反应中的氧化剂是二氧化锰.