题目内容
17.除去FeCl3溶液中混有的少量FeCl2,可以向此溶液中通入过量的氯气,发生如下反应:2FeCl2+Cl2═2FeCl3.对于该反应说法正确的是( )| A. | 属于氧化还原反应 | B. | 属于复分解反应 | ||
| C. | Cl2作还原剂 | D. | Fe2+被还原 |
分析 2FeCl2+Cl2═2FeCl3反应中Fe元素的化合价升高,Cl元素的化合价降低,据此分析.
解答 解:该反应中存在元素化合价的变化,属于氧化还原反应,2FeCl2+Cl2═2FeCl3反应中Fe元素的化合价升高,则Fe2+被氧化,Cl元素的化合价降低,Cl2作氧化剂,故A正确.
故选A.
点评 本题考查混了铁的化合物的性质、氧化还原反应,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
7.对三联苯是一种有机合成的中间体.工业上合成对三联苯的化学方程式为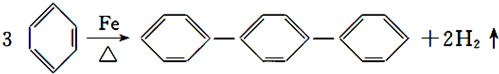
下列说法中正确的是( )

下列说法中正确的是( )
| A. | 上述反应属于取代反应 | |
| B. | 对三联苯分子中至少有18个原子共平面 | |
| C. | 对三联苯的一氯取代物有4种 | |
| D. | 0.2 mol对三联苯在足量的氧气中完全燃烧消耗5.1 mol O2 |
8.已知四种短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同电子层结构,则下列叙述不正确的是( )
| A. | 原子半径 B>A>C>D | B. | 最高价氧化物水化物的碱性B>A | ||
| C. | 离子半径 C3->D->B+>A2+ | D. | 氢化物的稳定性 C>D |
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 某澄清透明溶液中:K+、Fe3+、NO3-、Cl- | |
| B. | 含0.1mol•L-1 Ba2+的溶液中:Na+、K+、SO42-、Cl- | |
| C. | 含0.1mol•L-1 CO32-的溶液中:OH-、Cl-、NH4+、Na+ | |
| D. | 加入铝粉产生H2的溶液中:Al3+、Na+、SO42-、NO3- |
2.下列说法正确的是( )
| A. | CH4的摩尔质量为16g | |
| B. | 标准状况下,18 g H2O的体积是22.4 L | |
| C. | 17 g NH3的物质的量是1 mol | |
| D. | 阿伏加德罗常数约为6.02×1023 |
9.下列说法中正确的是( )
| A. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 | |
| B. | 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子之间的作用力 | |
| C. | 烧碱固体溶于水的过程中,共价键被破坏 | |
| D. | 有机化合物CH3CH2NO2与H2N-CH2-COOH是同分异构体 |
 H2S
H2S Na2O
Na2O H2O22H•+2
H2O22H•+2 →
→ .
.