��Ŀ����
2��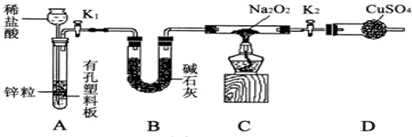 �ƵĻ������ڹ�ũҵ���������ǵ��ճ����������Ź㷺��Ӧ�ã�����Na2O2������Ư����DZˮͧ�еĹ�������Na2O2��ǿ�����ԣ�H2���л�ԭ�ԣ�ijͬѧ����������ԭ��Ӧ��֪ʶ�Ʋ�Na2O2��H2�ܷ�Ӧ��Ϊ����֤���Ʋ�������ͬѧ��Ʋ���������ʵ�飬ʵ�鲽����������£�
�ƵĻ������ڹ�ũҵ���������ǵ��ճ����������Ź㷺��Ӧ�ã�����Na2O2������Ư����DZˮͧ�еĹ�������Na2O2��ǿ�����ԣ�H2���л�ԭ�ԣ�ijͬѧ����������ԭ��Ӧ��֪ʶ�Ʋ�Na2O2��H2�ܷ�Ӧ��Ϊ����֤���Ʋ�������ͬѧ��Ʋ���������ʵ�飬ʵ�鲽����������£�����1������ͼ��װ������ͼ�мг�����ʡ�ԣ������װ�õ������ԣ�Ȼ��װ��ҩƷ��
����2����K1��K2������������������װ��Na2O2��Ӳ�ʲ����ܵĹ����У�û�й۲쵽�κ�����
����3��������H2�Ĵ��Ⱥ�ȼ�ƾ��Ƽ��ȣ��۲쵽Ӳ�ʲ�������Na2O2���ۻ�������ɫ�ķ�ĩ��������˰�ɫ���壬�����������ͭδ����ɫ��
����4����Ӧ��ȥ�ƾ��ƣ���Ӳ�ʲ�������ȴ��ر�K1��
����������Ϣ�ش��������⣺
��1����װ��������Ҫ���װ�õ������ԣ��������K2֮ǰװ�������Եķ����ر�K2����K1���ӳ���©���м�ˮ��������Һ������Թ�Һ��
һ��ʱ���Һ���䣬˵�����������ã�����Aװ���Ʊ�������ŵ����������ƻ��濪���ã�д��1�㼴�ɣ���ʵ��������Aװ�û������Ʊ���������H2S��CO2��д��1�ּ��ɣ���
��2��ʢװCuSO4ҩƷ�����������Ǹ���ܣ�Bװ�õ������dz�ȥ�����е��Ȼ����ˮ������
��3����������������ȵ�ԭ���Ƿ�ֹ������������ϼ��ȱ�ը��
��4������װ��D��Ŀ���Ǽ�������ˮ���ɣ�
��5��������ʵ����Ƴ�Na2O2��H2��Ӧ�Ļ�ѧ����ʽΪNa2O2+H2$\frac{\underline{\;\;��\;\;}}{\;}$2NaOH��
���� Ϊ�Ʋ�Na2O2��H2�ܷ�Ӧ����ѡҪ�Ƶ�������AΪ�������Ʊ�װ�ã�ʵ������п��ϡ���ᷴӦ���������Ƶõ������к��Ȼ������塢ˮ��������B��ʯ�����գ�C��Na2O2��H2�ķ�Ӧװ�ã�D����������Ƿ���ˮ���ɣ�
��1������ʵ�����м��װ�õ������Եķ����أ���ϵ���շ�����ԭ���ش���ϵ���ʵ�����Իش�
��2������ʵ���ҳ����������ƻش����ݸ���ܵ����ûش�
��3���������������ױ�ը�ش�
��4������CuSO4�����ûش�
��5�����ݹ������Ƶ��������������ڸ����µĻ�ԭ���Լ�ʵ�����������
��� �⣺Ϊ�Ʋ�Na2O2��H2�ܷ�Ӧ����ѡҪ�Ƶ�������AΪ�������Ʊ�װ�ã�ʵ������п��ϡ���ᷴӦ���������Ƶõ������к��Ȼ������塢ˮ��������B��ʯ�����գ�C��Na2O2��H2�ķ�Ӧװ�ã�D����������Ƿ���ˮ���ɣ�
��1�������װ�������Եķ���Ϊ���ر�K2����K1���ӳ���©���м�ˮ��������Һ������Թ�Һ�棬һ��ʱ���Һ���䣬˵�����������ã�����Aװ���Ʊ�������ŵ��ǣ��������ƻ��濪���ã�Aװ�������ڹ�����Һ�岻���ȿ�����ȡ�����壬�ʿ�����H2S����CO2��
�ʴ�Ϊ���ر�K2����K1���ӳ���©���м�ˮ��������Һ������Թ�Һ�棬һ��ʱ���Һ���䣬˵�����������ã��������ƻ��濪���ã�H2S��CO2��
��2��ʢװCuSO4ҩƷ�����������ǣ�����ܣ�Bװ�õ������ǣ���ȥ�����е��Ȼ����ˮ��������ӣ�
�ʴ�Ϊ������ܣ���ȥ�����е��Ȼ����ˮ������
��3������ȼ�ױ�ը��ҩƷ������м��鴿�ȣ�
�ʴ�Ϊ����ֹ������������ϼ��ȱ�ը��
��4��CuSO4�ǰ�ɫ��ĩ����ˮ�����ɫ���壬�ʳ���CuSO4�����Ƿ���ˮ��
�ʴ�Ϊ����������ˮ���ɣ�
��5��������������Ԫ�ؾ��������ԣ��������ڸ����¾��л�ԭ�ԣ��Ҹ����������ͭδ����ɫ��˵��û��ˮ���ɣ��ʷ�ӦΪNa2O2+H2=2NaOH��
�ʴ�Ϊ��Na2O2+H2$\frac{\underline{\;\;��\;\;}}{\;}$2NaOH��
���� ������Ҫ�������ʵ���ҳ��������Լ������Եļ�顢����ͭ�����ʡ��������Ƶ����ʵȣ��Ѷ����У�

 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�| A�� | �����е�2��Ԫ�ص�ԭ���������2������ | |
| B�� | ��3��12��Ԫ��ȫΪ���� | |
| C�� | ��3��Ԫ��������� | |
| D�� | ��15��16��17��Ԫ�ض��Ƿǽ���Ԫ�� |
| A�� | Naͨ��������ú���У���ͬ���Liֻ�ܱ�����Һ��ʯ���� | |
| B�� | ���ʯ��ʯī��Ϊͬ�������壬��֪ ȼ���Ƚ��ʯ���ߣ���ʯī�Ƚ��ʯ���ȶ� | |
| C�� | X�Ļ�ѧʽΪNa2CO3����Mg ��CO2������MgO��C | |
| D�� | ����0.4molNa���뷴Ӧʱ����������CO2Ϊ0.3NA |
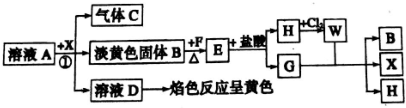
 ��G�л�ѧ��������Ϊ���Թ��ۼ���
��G�л�ѧ��������Ϊ���Թ��ۼ���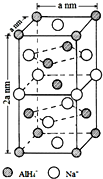
 ����
����
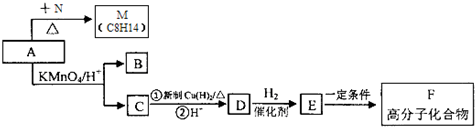


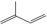 ��д������A��ͬһ��������Ҵ���˳���칹���л���ṹ��ʽCH3CH=CHCH=CH2��
��д������A��ͬһ��������Ҵ���˳���칹���л���ṹ��ʽCH3CH=CHCH=CH2�� ��
��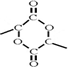 ��
��