题目内容
12.向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成血红色.该反应在有的教材中用方程式FeCl3+3KSCN═Fe(SCN)3+3KCl表示.经研究表明,Fe(SCN)3是配合物.Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合.请按要求填空:①Fe3+与SCN-反应时,Fe3+提供空轨道,SCN-提供孤对电子,二者通过配位键结合.
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显血红色.含该离子的配合物的化学式是[Fe(SCN)]Cl2.
③若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在溶液中发生反应的化学方程式可以表示为FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl.
分析 ①形成配位键的条件是中心离子或原子含有空轨道,配体含有孤对电子;
②Fe3+与SCN-以个数比1:1配合所得离子为[Fe(SCN)]2+,故FeCl3与KSCN在水溶液中反应生成[Fe(SCN)]Cl2与KCl;
③Fe3+与SCN-以个数比1:5配合所得离子为[Fe(SCN)5]2-,故FeCl3与KSCN在水溶液中反应生成K2[Fe(SCN)5]与KCl.
解答 解:①Fe3+与SCN-反应生成的配合物中,Fe3+提供空轨道,SCN-提供孤对电子,
故答案为:空轨道,孤对电子;
②Fe3+与SCN-以个数比1:1配合所得离子为[Fe(SCN)]2+,故FeCl3与KSCN在水溶液中反应生成[Fe(SCN)]Cl2与KCl,
故答案为:[Fe(SCN)]Cl2;
③Fe3+与SCN-以个数比1:5配合所得离子为[Fe(SCN)5]2-,故FeCl3与KSCN在水溶液中反应生成K2[Fe(SCN)5]2-与KCl,所以反应方程式为:FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl,
故答案为:FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl.
点评 本题考查配合物知识,属于信息给予题目,关键是确定配离子,较好地考查学生对信息的获取与知识迁移运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列说法不正确的是( )
| A. | 甲基的电子式为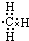 | |
| B. | 大量获得乙烯的工业方法是乙醇的消去反应 | |
| C. | C3H8只能表示一种物质 | |
| D. | 乙烷在光照的条件下与氯气混和,最多可以生成10种物质 |
3.下列说法一定正确的是( )
| A. | 其水溶液导电的一定是离子晶体 | |
| B. | 固态导电的一定是金属晶体 | |
| C. | 共价化合物形成的晶体一定是分子晶体 | |
| D. | 固态不导电、熔融态导电的一定是离子晶体 |
9.下列各组有机物的鉴别(括号内为鉴别试剂)不合理的是( )
| A. | 苯、甲苯、溴乙烷(酸性高锰酸钾溶液) | B. | 乙醇、乙醛、乙酸(新制Cu(OH)2 | ||
| C. | 苯、乙醇、四氯化碳(水) | D. | 苯、己烷、苯酚溶液(浓溴水) |
6.下列各组顺序的排列不正确的是( )
| A. | 熔点:Li>Na>K | B. | 还原性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H2SO4 | D. | 原子半径:Na<Mg<Al |
7.下列说法正确的是( )
| A. | 为了防止中秋月饼的富脂食物因被氧化而变质,常在包装袋里放还原铁粉 | |
| B. | 天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点 | |
| C. | 麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖 | |
| D. | 若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
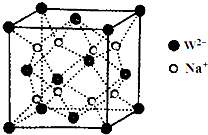 前四周期元素X、Y、Z、W、R、Q的原子序数依次增大,X的核外电子总数与其周期数相同;Y有三个能级,且每个能级上的电子数相等;Z原子单电子数在同周期元素中最多;W与Z同周期,第一电离能比Z的低;R与Y同一主族,Q的最外层电子数为2,其他电子层电子均处于饱和状态.请回答下列问题:
前四周期元素X、Y、Z、W、R、Q的原子序数依次增大,X的核外电子总数与其周期数相同;Y有三个能级,且每个能级上的电子数相等;Z原子单电子数在同周期元素中最多;W与Z同周期,第一电离能比Z的低;R与Y同一主族,Q的最外层电子数为2,其他电子层电子均处于饱和状态.请回答下列问题: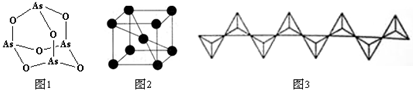
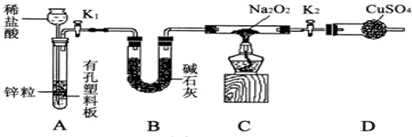 钠的化合物在工农业生产和人们的日常生活中有着广泛的应用,其中Na2O2常用作漂白剂和潜水艇中的供氧剂.Na2O2有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能反应.为了验证此推测结果,该同学设计并进行如下实验,实验步骤和现象如下.
钠的化合物在工农业生产和人们的日常生活中有着广泛的应用,其中Na2O2常用作漂白剂和潜水艇中的供氧剂.Na2O2有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能反应.为了验证此推测结果,该同学设计并进行如下实验,实验步骤和现象如下.