题目内容
1.已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润的红色石蕊试纸变蓝的气体,它们之间能发生如下反应:①A+H2O→B+C;
②F+C→D (白烟);
③D+NaOH$\stackrel{△}{→}$ E+F+H2O.
(1)写出它们的化学式:
ANO2,CHNO3,DNH4NO3,FNH3.
(2)写出下列反应的化学方程式,并按要求填空:
②NH3+HNO3=NH4NO3,这个反应不属于(填“属于”或“不属于”)氧化还原反应;
(3)工业生产C的过程中有一步反应为F经催化氧化生成B和H2O,写出该步反应的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
分析 F是能使红色湿润石蕊试纸变蓝的气体,则F为NH3,由③D+NaOH→F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,FC反应生成D冒白烟,反应生成的D是NH4NO3,根据②C+F→D,可知C是HNO3,再根据①A+H2O→B+C,则A是NO2,B是NO,据此解答.
解答 解:F是能使红色湿润石蕊试纸变蓝的气体,则F为NH3,由③D+NaOH→F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,FC反应生成D冒白烟,反应生成的D是NH4NO3,根据②C+F→D,可知C是HNO3,再根据①A+H2O→B+C,则A是NO2,B是NO,
(1)由上分析,A为NO2,C为HNO3,D为NH4NO3,F为NH3,
故答案为:NO2;HNO3;NH4NO3;NH3;
(2)反应②的化学方程式为:NH3+HNO3=NH4NO3,反应前后无元素化合价变化不是氧化还原反应,
故答案为:NH3+HNO3=NH4NO3;不属于;
(3)NH3经催化氧化生成NO和H2O,反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
点评 本题考查无机物推断,涉及N元素化合物性质与转化,F是能使红色湿润石蕊试纸变蓝的气体是推断突破口,再结合转化关系分析推断,题目难度中等,侧重对学生基础知识的巩固与训练.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列实验操作正确的是( )
| A. | 制取蒸馏水时,为了防止瓶内产生暴沸现象,应先向烧瓶内加入几片碎瓷片 | |
| B. | 稀释浓硫酸时,常把水加入到盛浓硫酸的烧杯中 | |
| C. | 做CO还原Fe2O3实验时,为防止CO污染环境,实验完毕,常先停止通CO,再停止加热 | |
| D. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
12.下列关于化学键的叙述,正确的一项是( )
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 全部由非金属元素形成的化合物中不可能含有离子键 | |
| D. | 含有共价键的化合物一定是共价化合物 |
13.既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有乙烯的方法是( )
| A. | 通入足量的溴水 | B. | 通入足量的酸性高锰酸钾溶液 | ||
| C. | 在导管口点燃 | D. | 一定条件下与H2反应 |
10.下列化工生产过程中所发生的主要化学反应不属于氧化还原反应的是( )
| A. | 用氯气和氢氧化钠溶液制消毒水 | B. | 用铝热法冶炼金属钒 | ||
| C. | 用油脂制肥皂 | D. | 海水提溴 |
11.下列事实能证明甲烷分子是以碳原子为中心的正四面体结构的是( )
| A. | 四个C-H键完全相同 | B. | CH4的一氯代物只有一种 | ||
| C. | CH2Cl2只有一种空间结构 | D. | 在常温常压下CH2Cl2为液体 |
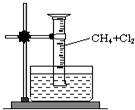 某研究小组为了探究甲烷和氯气反应的情况,设计了如下实验.请填写下列空白:
某研究小组为了探究甲烷和氯气反应的情况,设计了如下实验.请填写下列空白: