题目内容
16.某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.
(1)利用I、Ⅱ装置可制取收集气体(K2关闭,K1打开)
①下列各组物质中能直接利用这套装置进行实验的是AC (填标号)
A.锌和稀硫酸B.双氧水和二氧化锰
C.浓氨水和氧化钙D.浓盐酸和二氧化锰
②在不改变I、II装置及位置的前提下,若要制取收集NO气体,可采取的改进方法是将装置II内充满水;
(2)利用I、III装置可验证物质的性质(K2打开,K1关闭)
①若要证明氧化性:KMnO4>C12>Br2,则A中加浓盐酸,B中加KMnO4,C中发生的离子反应方程式Cl2+2Br-=2Cl-+Br2.
②若要证明乙烯为不饱和烃,C中的现象为溴水或溴的四氯化碳溶液褪色.
分析 (1)①根据反应装置、气体收集装置的特点选择;
②根据二氧化氮的性质选取试剂;
(2)①根据氯气和溴之间的置换反应判断氧化性强弱,并写出相应的离子方程式;
②根据碳化钙和水的反应写出相应的方程式;根据乙炔与溴水或酸性高锰酸钾反应的现象判断.
解答 解:(1)①根据I装置知,反应物反应时不需加热,所以D排除;根据Ⅱ装置知,反应生成的气体密度小于空气的密度,所以排除B,符合条件的是AC.
故选AC.
②二氧化氮能和水反应,所以不能用排水法收集,可将Ⅱ装置加满(难挥发的)有机溶剂来收集二氧化氮气体.
故答案为:将Ⅱ装置加满(难挥发的)有机溶剂.
(2)①氯气能和溴化物置换出溴单质Cl2+2Br-=2Cl-+Br2,从而确定氯气的氧化性大于溴的
故答案为:Cl2+2Br-=2Cl-+Br2.
②碳化钙和水反应生成氢氧化钙和乙炔,CaC2+2H2O→Ca(OH)2+C2H2↑;溴或酸性高锰酸钾有强氧化性,能氧化
乙炔,所以乙炔能使溴水或高锰酸钾溶液褪色.
故答案为:溴水褪色或高锰酸钾溶液褪色.
点评 本题考查了气体发生装置的选择,常见气体发生装置的选择依据是反应物的状态和反应条件,掌握物质性质和实验制备方法是解题关键,题目难度中等.

练习册系列答案
相关题目
6.下列说法正确的是( )
| A. | 华北地区水资源十分匮乏,必须节约用水 | |
| B. | 明矾能沉降水中的悬浮物,又能杀菌消毒 | |
| C. | 活性炭既可以吸附水中的异味,又可以降低水的硬度 | |
| D. | 长期饮用纯净水,不利于人体健康 |
4.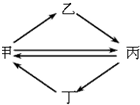 如图是甲、乙、丙、丁四种物质的转化关系,其中每一步都能一步实现的是( )
如图是甲、乙、丙、丁四种物质的转化关系,其中每一步都能一步实现的是( )
 如图是甲、乙、丙、丁四种物质的转化关系,其中每一步都能一步实现的是( )
如图是甲、乙、丙、丁四种物质的转化关系,其中每一步都能一步实现的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | FeCl3 | FeCl2 | Fe2O3 | Fe(OH)3 |
| B | Cu | CuO | CuSO4 | CuCl2 |
| C | NO | HNO3 | NO2 | NH3 |
| D | Si | Na2SiO3 | SiO2 | SiF4 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
1.下列叙述中正确的是( )
| A. | 在稀溶液中1mol酸和1mol碱完全反应所放出的热量,叫做中和热 | |
| B. | 在101kP时1mol物质燃烧时所放出的热量叫做该物质的燃烧热 | |
| C. | 热化学方程式中,各物质前的化学计量数不表示分子个数 | |
| D. | 在相同条件下,1 molH20(l)完全分解吸收的热量与H2、O2化合生成1 molH2O(g)放出的热量数值相等 |
8.下列说法正确的是( )
| A. | 烃是指含有碳、氢元素的化合物 | |
| B. | 烷烃的特征反应是取代反应和氧化反应 | |
| C. | 乙烯聚合后的产物是混合物 | |
| D. | 乙烷与氯气取代后的产物一定是纯净物 |
 .
.