题目内容
6.现有V L K2SO4和Al2(SO4)3的混合溶液,已知其中c(Al3+)为0.4mol/L,c (K+)为0.2mol/L,则溶液中SO42-的物质的量浓度为( )| A. | 0.2mol/L | B. | 0.4 mol/L | C. | 0.8mol/L | D. | 0.7mol/L |
分析 任何电解质溶液中都存在电荷守恒,根据电荷守恒得3c(Al3+)+c (K+)=2c(SO42-),则c(SO42-)=$\frac{3c(A{l}^{3+})+c({K}^{+})}{2}$.
解答 解:任何电解质溶液中都存在电荷守恒,根据电荷守恒得3c(Al3+)+c (K+)=2c(SO42-),则c(SO42-)=$\frac{3c(A{l}^{3+})+c({K}^{+})}{2}$=$\frac{0.4×3+0.2}{2}$mol/L=0.7mol/L,
故选D.
点评 本题考查物质的浓度计算,为高频考点,侧重考查学生分析计算能力,明确溶液中存在的电荷守恒是解本题关键,注意“3c(Al3+)+c (K+)=2c(SO42-)“中3、2的含义,题目难度不大.

练习册系列答案
相关题目
14.不能用有关胶体的观点解释的现象是( )
| A. | 在NaCl溶液中滴入AgNO3溶液有沉淀 | |
| B. | 同一钢笔同时使用不同牌号的墨水易发生堵塞 | |
| C. | 在河流入海口易形成三角洲 | |
| D. | 在实验中不慎手被玻璃划破,可用FeCl3溶液应急止血 |
11.海带中碘元素的检验可经过以下四个步骤完成(已知H2O2在酸性条件下能将海带中的I?氧化成I2,I2遇淀粉变蓝),各步骤中选用的实验用品不正确的是( )
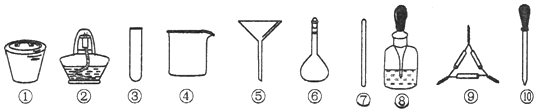

| A. | 将海带剪碎后灼烧成灰,选用①、②和⑨ | |
| B. | 将海带灰加蒸馏水溶解,选用④、⑥和⑦ | |
| C. | 过滤得到滤液,选用④、⑤和⑦ | |
| D. | 取滤液,先加入几滴稀硫酸,再滴加H2O2,最后滴加淀粉溶液,选用③和⑩ |
15.下列各组物质中,前者是单质,后者是氧化物的是( )
| A. | 水 碱石灰 | B. | 金刚石 干冰 | C. | 液氧 氯酸钾 | D. | 汞 纯碱 |
16.下列反应中,氧化剂与还原剂物质的量的关系不是1:2的是( )
| A. | 3S+6NaOH═Na2SO3+2Na2S+3H2O | |
| B. | 3NO2+H2O═2HNO3+NO | |
| C. | 2FeCl2+Cl2=3FeCl3 | |
| D. | 4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O |
 硫在空气中燃烧可以生成SO2,SO2在催化剂作用下可以被氧化为SO3,其热化学方程式可表示为:S(g)+O2(g)═SO2(g)△H=-297kJ/mol,SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-98.3kJ/mol.如图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6mol SO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量.
硫在空气中燃烧可以生成SO2,SO2在催化剂作用下可以被氧化为SO3,其热化学方程式可表示为:S(g)+O2(g)═SO2(g)△H=-297kJ/mol,SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-98.3kJ/mol.如图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6mol SO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量.