题目内容
使相同体积的NaCl、CaCl2、AlCl3溶液中的Cl-全部沉淀,用去同浓度的AgNO3溶液的体积分别为3V、2V、V,则NaCl、CaCl2、AlCl3溶液的物质的量浓度之比为 .
考点:物质的量浓度的相关计算
专题:计算题
分析:假设硝酸银的物质的量浓度为cmol/L,完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗相同浓度的AgNO3溶液的体积分别为3V、2V、V,发生反应Ag++Cl-=AgCl↓,设NaCl、MgCl2、AlCl3溶液的浓度分别为x、y、z,溶液体积为n L,根据方程式列式计算NaCl、CaCl2、AlCl3溶液的物质的量浓度之比.
解答:
解:假设硝酸银的物质的量浓度为cmol/L,完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗相同浓度的AgNO3溶液的体积分别为3V、2V、V,
设NaCl、MgCl2、AlCl3溶液的浓度分别为xmol/L、ymol/L、zmol/L,溶液体积为n L,
根据反应Ag++Cl-=AgCl↓可得:3V×c=nL×x、2V×c=2y×n L,Vc=3z×n L,
故x:y:z=
:
:
=3:1:
=9:3:1,
故答案为:9:3:1.
设NaCl、MgCl2、AlCl3溶液的浓度分别为xmol/L、ymol/L、zmol/L,溶液体积为n L,
根据反应Ag++Cl-=AgCl↓可得:3V×c=nL×x、2V×c=2y×n L,Vc=3z×n L,
故x:y:z=
| 3Vc |
| n |
| Vc |
| n |
| Vc |
| 3n |
| 1 |
| 3 |
故答案为:9:3:1.
点评:本题考查了物质的量浓度的计算、离子方程式的有关计算,题目难度不大,注意掌握物质的量浓度的概念及计算方法,明确发生的离子反应是解题关键.

练习册系列答案
相关题目
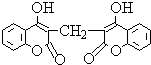 某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )| A、有望将它发展制得一种抗凝血药 |
| B、它无嗅并略具芳香味,因而可用来制备致命性出血型的杀鼠药 |
| C、它可由化合物和甲醛(HCHO)通过缩合反应制得 |
| D、它易溶于水、乙醇、乙醚等有机溶剂 |
下列分离提纯方法不正确的是( )
| A、分离硝酸钾和氯化钠,常用结晶与重结晶 |
| B、提纯含有碘的食盐,常用升华法 |
| C、去除乙醇中的水常用蒸馏法 |
| D、分离苯和四氯化碳可用分液法 |
分离NaCl、FeCl3和BaSO4的混合物,应选用的一组试剂是( )
| A、H2O、AgNO3、HNO3 |
| B、H2O、NaOH、HNO3 |
| C、H2O、NaOH、HCl |
| D、H2O、KOH、HNO3 |
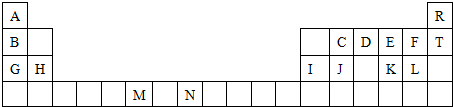
 所示,该晶胞中含有金属原子的数目为
所示,该晶胞中含有金属原子的数目为