题目内容
分离NaCl、FeCl3和BaSO4的混合物,应选用的一组试剂是( )
| A、H2O、AgNO3、HNO3 |
| B、H2O、NaOH、HNO3 |
| C、H2O、NaOH、HCl |
| D、H2O、KOH、HNO3 |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:要进行物质的分离,需根据物质的性质的不同进行.氯化铁能与碱反应生成氢氧化铁沉淀,然后与盐酸反应重新生成氯化铁.硫酸钡不溶于水,
解答:
解:三种物质中,硫酸钡不溶于水,故先加水过滤能将硫酸钡分离出来,
要分离氯化铁和氯化钠,需要先将其中的氯化铁转化为氢氧化铁沉淀,此时所选的试剂与氯化铁反应不能生成新的杂质,故可以选用NaOH,
然后将生成的氢氧化铁沉淀过滤即可分离得到氯化钠,向生成的氢氧化铁沉淀中加入盐酸即可生成氯化铁,
故选:C.
要分离氯化铁和氯化钠,需要先将其中的氯化铁转化为氢氧化铁沉淀,此时所选的试剂与氯化铁反应不能生成新的杂质,故可以选用NaOH,
然后将生成的氢氧化铁沉淀过滤即可分离得到氯化钠,向生成的氢氧化铁沉淀中加入盐酸即可生成氯化铁,
故选:C.
点评:本题考查了常见物质的分离,进行此类题目时,要根据物质的性质选择合适的试剂,要求分离过程中不能生成新的杂质,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
已知16g A物质和12g B物质恰好完全反应,生成6.8g C物质、3.6g D物质和0.2mol E物质,则E物质的摩尔质量为( )
| A、48g/mol |
| B、88g/mol |
| C、112g/mol |
| D、132g/mol |
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器I(恒容)和Ⅱ(恒压)中,使其发生反应,t.时容器I中达到化学平衡,x、Y、z的物质的量的变化如图所示,则下列有关推断正确的是( )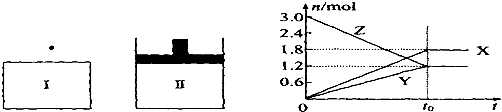

| A、该反应的化学方程式为:3X+2Y?3Z |
| B、若两容器中均达到平衡后,两容器的体积V(I)<V(Ⅱ),则容器Ⅱ达到平衡所用时间小于t |
| C、若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态 |
| D、达平衡后,若对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应 |
下列关于乙醇和乙酸的说法中,正确的是( )
| A、乙醇和乙酸在一定条件下能发生酯化反应 |
| B、乙酸能溶于水,但不溶于乙醇 |
| C、乙醇和乙酸均能使紫色石蕊试液变红 |
| D、乙醇和乙酸分子中都含有C=O键 |