题目内容
 将1mol I2(g) 和2mol H2置于2L密闭容器中,在一定温度下发生反应:
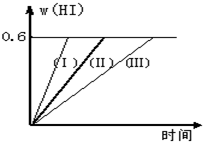
将1mol I2(g) 和2mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g);△H<0,并达平衡.HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
(1)达平衡时,H2 (g)的物质的量浓度为
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示.则甲条件可能是
(填入下列条件的序号)
①恒容条件下,升高温度;
②恒容条件下,降低温度;
③恒温条件下,缩小反应容器体积;
④恒温条件下,扩大反应容器体积;
⑤恒温恒容条件下,加入适当催化剂.
⑥向容器中再充入1mol I2(g) 和2mol H2
(3)若保持温度不变,在另一个相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,则a、b、c的关系是
考点:化学平衡的计算,化学平衡的影响因素,产物的百分含量随浓度、时间的变化曲线
专题:化学平衡专题
分析:(1)根据碘化氢的体积分数计算平衡时碘化氢的物质的量,再根据碘化氢和氢气之间的关系式计算剩余的氢气;
(2)反应时间发生变化,但碘化氢的含量不变,说明该条件只改变反应速率不影响平衡,压强和催化剂对该反应平衡无影响;
(3)运用等效平衡判断,恒温恒容,前后气体体积不变化,按化学计量数转化到左边,满足与原来加入的反应物物质的量比例相等即可.
(2)反应时间发生变化,但碘化氢的含量不变,说明该条件只改变反应速率不影响平衡,压强和催化剂对该反应平衡无影响;
(3)运用等效平衡判断,恒温恒容,前后气体体积不变化,按化学计量数转化到左边,满足与原来加入的反应物物质的量比例相等即可.
解答:
解:(1)该反应是一个反应前后气体体积不变的化学反应,所以反应后混合气体的物质的量是3mol,同一容器中各种气体的体积分数等其物质的量分数,所以平衡时碘化氢的物质的量=3mol×0.6=1.8mol,则参加反应的n(H2)=0.5n(HI)=0.5×1.8=0.9mol,剩余的n(H2)=2-0.9=1.1mol,所以平衡时c(H2)=
=0.55mol/L,
故答案为:0.55mol/L;
(2)在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,反应时间缩短,碘化氢的含量不变,说明该条件只增大了反应速率不影响平衡,增大压强(缩小反应容器体积)和加入催化剂对该反应平衡无影响,但都增大反应速率,缩短反应时间;
在乙条件下w(HI)的变化如曲线(Ⅲ) 所示,反应时间变长,碘化氢的含量不变,说明反应速率减小,平衡不移动,所以是减小压强(扩大容器体积),
故答案为:③⑤;④;
(3)若保持温度不变,在另一个相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,与原来的平衡是等效平衡,恒温恒容,前后气体体积不变化,按化学计量数转化到左边,满足与原来加入的反应物物质的量比例相等即可;
I2(g)+H2(g)?2HI(g);
开始(mol):a b c
变化(mol):0.5c 0.5c c
平衡(mol):a+0.5c b+0.5c 0
则(a+0.5c ):( b+0.5c)=1:2,
所以4a+c=2b,
故答案为:4a+c=2b.
| 1.1 |
| 2 |
故答案为:0.55mol/L;
(2)在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,反应时间缩短,碘化氢的含量不变,说明该条件只增大了反应速率不影响平衡,增大压强(缩小反应容器体积)和加入催化剂对该反应平衡无影响,但都增大反应速率,缩短反应时间;
在乙条件下w(HI)的变化如曲线(Ⅲ) 所示,反应时间变长,碘化氢的含量不变,说明反应速率减小,平衡不移动,所以是减小压强(扩大容器体积),
故答案为:③⑤;④;
(3)若保持温度不变,在另一个相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,与原来的平衡是等效平衡,恒温恒容,前后气体体积不变化,按化学计量数转化到左边,满足与原来加入的反应物物质的量比例相等即可;
I2(g)+H2(g)?2HI(g);
开始(mol):a b c
变化(mol):0.5c 0.5c c
平衡(mol):a+0.5c b+0.5c 0
则(a+0.5c ):( b+0.5c)=1:2,
所以4a+c=2b,
故答案为:4a+c=2b.
点评:本题考查外界条件对化学平衡的影响,等效平衡等知识点,注意碘和氢气的反应特点及等效平衡的应用.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
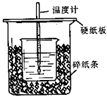 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: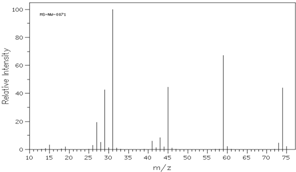
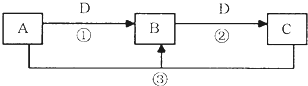
 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题.