题目内容
某有机物含有C、H、O三种元素.经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%.如图是该有机物的质谱图.该有机物的相对分子质量 则该有机物的分子式为 .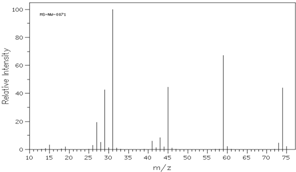

考点:有关有机物分子式确定的计算
专题:有机化学基础
分析:(1)根据质谱图中数据判断该有机物的相对分子量;
(2)计算出氧元素的质量分数,然后计算出C、H、O元素的物质的量之比,从而得出其实验式,再根据其相对分子量计算出其分子式.
(2)计算出氧元素的质量分数,然后计算出C、H、O元素的物质的量之比,从而得出其实验式,再根据其相对分子量计算出其分子式.
解答:
解:(1)根据质谱图可知,该有机物的相对分子质量为74,
故答案为:74;
(2)碳的质量分数是64.86%,氢的质量分数是13.51%,氧元素质量分数为:1-64.86%-13.52=21.63%,则该物质中碳、氢、氧原子个数之比=
:
:
=4:10:1,所以其实验式为:C4H10O,该实验式的式量为74,该有机物的相对分子质量为74,则该有机物的分子式与实验式相同,都是C4H10O,
故答案为:C4H10O.
故答案为:74;
(2)碳的质量分数是64.86%,氢的质量分数是13.51%,氧元素质量分数为:1-64.86%-13.52=21.63%,则该物质中碳、氢、氧原子个数之比=
| 64.86% |
| 12 |
| 13.51% |
| 1 |
| 21.63% |
| 16 |
故答案为:C4H10O.
点评:本题考查了有机物实验式、分子式的确定,题目难度中等,注意掌握有机物分子式的计算方法,明确质谱图的含义,能够根据质谱图判断物质的相对分子量.

练习册系列答案
相关题目
下列各项中,电离方程式正确的是( )
| A、HCO3-+H2O═CO32-+H3O + |
| B、H2SO3=2H++SO32- |
| C、NaHCO3═Na++HCO3- |
| D、NaHSO4(熔融)=Na++H++SO42- |
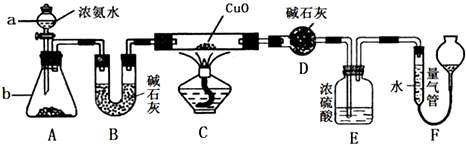
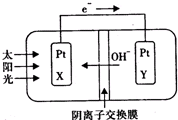 近年来C02的利用日新月异.
近年来C02的利用日新月异.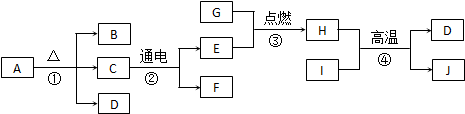
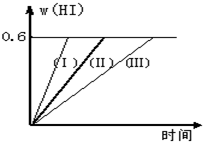 将1mol I2(g) 和2mol H2置于2L密闭容器中,在一定温度下发生反应:
将1mol I2(g) 和2mol H2置于2L密闭容器中,在一定温度下发生反应: