题目内容
5.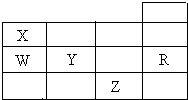 如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )
如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )| A. | XZ3是平面正三角形分子 | |
| B. | 钠与X形成的化合物Na3X和NaX3都是含有共价键的离子晶体 | |
| C. | W与Y元素的最高价氧化物对应的水化物酸性前者弱于后者 | |
| D. | X的氢化物比W的氢化物稳定,但沸点前者比后者低 |
分析 图为元素周期表前四周期的一部分,由元素的位置可知,X为N,W为P,Y为S,R为Ar,Z为Br,
A.XZ3是NBr3,立体构型为三角锥形;
B.Na3N中无共价键;
C.同周期元素从左到右,非金属性逐渐增强,非金属性越强最高价含氧酸的酸性越强;
D.同主族自上而下,非金属性减弱,非金属性越强,氢化物越稳定;氢键使沸点升高.
解答 解:图为元素周期表前四周期的一部分,由元素的位置可知,X为N,W为P,Y为S,R为Ar,Z为Br,则:
A.XZ3是NBr3,NBr3中N形成3个δ键,孤对电子数为$\frac{1}{2}$(5-3×1)=1,为sp3杂化,含有一个孤对电子,立体构型为三角锥形,故A错误;
B.Na3N中无共价键,故B错误;
C.同周期元素从左到右,非金属性逐渐增强,所以非金属性Y>W,则Y元素最高价氧化物对应水化物的酸性比W元素的最高价氧化物对应水化物的酸性强,故C正确;
D.同主族自上而下,非金属性减弱,所以非金属性X>W,非金属性越强,氢化物越稳定,所以氢化物的稳定性X>W;X的氢化物是氨气,氨气分子间存在氢键,使沸点相对较高,即X的氢化物比W的氢化物沸点高,故D错误;
故选:C.
点评 本题考查位置结构性质的关系及应用,利用元素的位置推断出元素是解答的关键,熟悉空间构型、化学键的判断、非金属性比较的方法及氢键的性质即可解答,题目难度中等.

练习册系列答案
相关题目
18.下列反应的离子方程式正确的是( )
| A. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | AgCl溶于氨水:AgCl+2NH3•H2O=[Ag(NH3)2]++Clˉ+2H2O | |
| C. | 向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO3 2- | |
| D. | 用稀硝酸除去试管内壁银:Ag+2H++NO3-=Ag++NO2↑+H2O |
13.下列有机物命名正确的是( )
| A. | 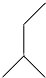 (2-乙基丙烷) (2-乙基丙烷) | B. | CH3CH2CH2CH2OH(1-丁醇) | ||
| C. |  (间二甲苯) (间二甲苯) | D. | CH3C(CH3)=CH2(2-甲基-2-丙烯) |
20. SOCl2是一种重要的化学试剂,常用作有机合成的氯化剂;利用SOCl2与水剧烈反应的性质,常用于金属水合氯化物的脱水剂;SOCl2还可作电池的正极材料.
SOCl2是一种重要的化学试剂,常用作有机合成的氯化剂;利用SOCl2与水剧烈反应的性质,常用于金属水合氯化物的脱水剂;SOCl2还可作电池的正极材料.
Ⅰ.一种制备SOCl2的常用方法是:SO3+SCl2=SOCl2+SO2,其模拟装置如图所示(夹持装置略去),各物质的部分性质如下:
(1)A装置是由水槽、温度计、蒸馏烧瓶和分液漏斗组装而成的,当蒸馏烧瓶中反应物出现
樱桃红色变为无色现象时,说明反应完成,停止滴加SO3.
(2)B中所盛药品是浓硫酸,装置C中药品及选择该药品的作用分别是氢氧化钠、吸收尾气.
(3)反应后将A中混合物进行蒸馏,收集到较纯净的产品,需控制蒸馏温度在C左右.
a.44.8℃b.59℃c.76℃
Ⅱ.Li-SOCl2电池是一种优质高效的电池,常放在心脏起搏器中,电池的总反应可表示为4Li+2SOCl2=4LiCl+S+SO2,回答下列问题:
(4)电池正极发生的电极反应为2SOCl2+4Li++4e-=4LiCl+S+SO2.
(5)该电池必须在惰性环境中组装,原因是锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应.
(6)若含金属锂6.9g的电池质量为m g,平均电压为n V,则该电池的比能量为$\frac{2.68×1{0}^{4}n}{m}$W•h•kg-1(用含有m、n的代数式,系数用科学计数法表示,结果保留三个有效数字:比能量=$\frac{电池输出电能}{电池质量}$,1W•h=3.6×103J,法拉第常数F=96500c•mol-1).
 SOCl2是一种重要的化学试剂,常用作有机合成的氯化剂;利用SOCl2与水剧烈反应的性质,常用于金属水合氯化物的脱水剂;SOCl2还可作电池的正极材料.
SOCl2是一种重要的化学试剂,常用作有机合成的氯化剂;利用SOCl2与水剧烈反应的性质,常用于金属水合氯化物的脱水剂;SOCl2还可作电池的正极材料.Ⅰ.一种制备SOCl2的常用方法是:SO3+SCl2=SOCl2+SO2,其模拟装置如图所示(夹持装置略去),各物质的部分性质如下:
| SO3 | SCl2 | SOCl2 | SO2 | |
| 熔点 | 16.8℃ | -122℃ | -104.5℃ | -75.5℃ |
| 沸点 | 44.8℃ | 59℃ | 76℃ | -10℃ |
| 颜色 | 无色 | 樱桃红色 | 无色 | 无色 |
| 备注 | 不稳定 | 不稳定,沸点以上分解 |
樱桃红色变为无色现象时,说明反应完成,停止滴加SO3.
(2)B中所盛药品是浓硫酸,装置C中药品及选择该药品的作用分别是氢氧化钠、吸收尾气.
(3)反应后将A中混合物进行蒸馏,收集到较纯净的产品,需控制蒸馏温度在C左右.
a.44.8℃b.59℃c.76℃
Ⅱ.Li-SOCl2电池是一种优质高效的电池,常放在心脏起搏器中,电池的总反应可表示为4Li+2SOCl2=4LiCl+S+SO2,回答下列问题:
(4)电池正极发生的电极反应为2SOCl2+4Li++4e-=4LiCl+S+SO2.
(5)该电池必须在惰性环境中组装,原因是锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应.
(6)若含金属锂6.9g的电池质量为m g,平均电压为n V,则该电池的比能量为$\frac{2.68×1{0}^{4}n}{m}$W•h•kg-1(用含有m、n的代数式,系数用科学计数法表示,结果保留三个有效数字:比能量=$\frac{电池输出电能}{电池质量}$,1W•h=3.6×103J,法拉第常数F=96500c•mol-1).
10.钛铁矿的主要成分为FeTiO3(可表示为FeO•TiO2).用浓盐酸溶解钛铁矿去渣得溶液(含有Fe2+、TiOCl42-等),调节溶液的pH并加热,过滤的TiO2和滤液.控制反应温度在95℃左右,向滤液中加入H2O2和NH4H2PO4得到FePO4.再将FePO4与Li2CO3和H2C2O4一起煅烧,可制取LiFePO4.有关数据如下表所示:
(1)FeTiO3中Ti的化合价为+4,盐酸与FeTiO3反应的离子方程式为FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O.检验溶液中Fe2+的方法是先滴加KSCN溶液,不显血红色,再加入过氧化氢,溶液显血红色.
(2)为提供FePO4的产率,根据上述制备方法和表中数据,应采取的正确措施是d(填正确答案的标号).
a.不加H2O2 b.调节溶液pH至5 c.降低反应温度 d.增大NH4H2PO4的用量
(3)磷的含氧酸H3PO2与足量的NaOH溶液反应,生成NaH2PO2.则H3PO2为一元酸;在LiFePO4中的化学键有离子键、共价键,在制备LiFePO4的过程中加入H2C2O4的作用是还原FePO4.
(4)LiFePO4可作锂电池的电极材料.充电时,Li+从LiFePO4晶格中迁移出来,部分LiFePO4转化为Li1-xFePO4,则阳极的电极反应式为LiFePO4-xe-═Li1-xFePO4+xLi+.
(5)电化学还原TiO2是获取金属钛的常用方法.采用熔融盐作电解质,用石墨作阳极,总反应为TiO2$\frac{\underline{\;电解\;}}{\;}$Ti+O2↑
①电解过程中,阳极不断被消耗而需要定期更换,其原因是2O2--4e-═O2↑,C+O2=CO2(用反应式表示).
②电解由含80%FeTiO3的钛铁矿制取的TiO2得到12kg金属钛,已知电流效率为76%,则至少需要该种钛铁矿62.5kg.(电流效率=$\frac{实际产量}{理论产量}$×100%)
| 化合物 | Fe(OH)2 | Fe(OH)3 | FePO4 | Fe3(PO4)2 |
| Ksp近似值 | 10-17 | 10-38 | 10-22 | 10-36 |
(2)为提供FePO4的产率,根据上述制备方法和表中数据,应采取的正确措施是d(填正确答案的标号).
a.不加H2O2 b.调节溶液pH至5 c.降低反应温度 d.增大NH4H2PO4的用量
(3)磷的含氧酸H3PO2与足量的NaOH溶液反应,生成NaH2PO2.则H3PO2为一元酸;在LiFePO4中的化学键有离子键、共价键,在制备LiFePO4的过程中加入H2C2O4的作用是还原FePO4.
(4)LiFePO4可作锂电池的电极材料.充电时,Li+从LiFePO4晶格中迁移出来,部分LiFePO4转化为Li1-xFePO4,则阳极的电极反应式为LiFePO4-xe-═Li1-xFePO4+xLi+.
(5)电化学还原TiO2是获取金属钛的常用方法.采用熔融盐作电解质,用石墨作阳极,总反应为TiO2$\frac{\underline{\;电解\;}}{\;}$Ti+O2↑
①电解过程中,阳极不断被消耗而需要定期更换,其原因是2O2--4e-═O2↑,C+O2=CO2(用反应式表示).
②电解由含80%FeTiO3的钛铁矿制取的TiO2得到12kg金属钛,已知电流效率为76%,则至少需要该种钛铁矿62.5kg.(电流效率=$\frac{实际产量}{理论产量}$×100%)
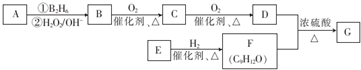
 ;该反应的反应类型为酯化反应或取代反应
;该反应的反应类型为酯化反应或取代反应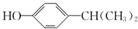
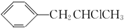 为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):
为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):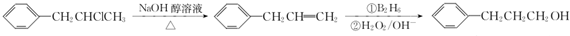 .
. .
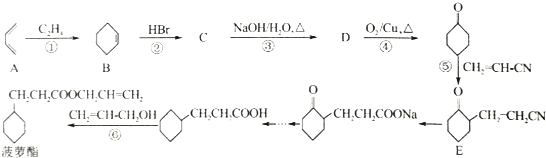
.
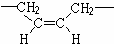 ,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.
,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.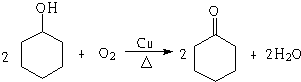 .
.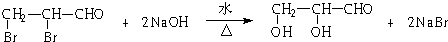 .
.