题目内容
19.已知2Mg(s)+O2(g)═2MgO(s)△Hθ=-1204kJ•mol-1计算:(1)生成每克MgO的反应热.
(2)要释放1kJ热量,必须燃烧多少克的Mg?
分析 (1)根据热化学方程式的含义可知生成2molMgO放出的热量为1204kJ计算;
(2)根据燃烧2mol镁放出1204kJ的热量计算.
解答 解:(1)2Mg(s)+O2(g)═2MgO(s)△H=-1204kJ•mol-1,根据热化学方程式的含义可知生成2molMgO放出的热量为1204kJ,即生成80gMgO放出的热量为1204kJ,生成毎克MgO放出的热量为:$\frac{1204kJ}{80}$=15.05kJ;
(2)燃烧2molMg放热1204kJ,即燃烧48gMg放热1204kJ,要释放1kJ热量需燃烧镁的质量为:$\frac{48g}{1204}$≈0.04g;
答:生成每克MgO放热15.05kJ;要释放1kJ热量,必须燃烧0.04gMg.
点评 本题考查反应热的计算,主要是明白热化学方程式的含义即可解答,题目比较简单.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
9.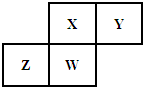 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是内层电子数的三倍.下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是内层电子数的三倍.下列说法不正确的是( )
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是内层电子数的三倍.下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是内层电子数的三倍.下列说法不正确的是( )| A. | Y元素与氢元素可形成H2Y2型的离子化合物 | |
| B. | Z元素的单质有半导体特性,原子半径:Z>X | |
| C. | 最高价氧化物对应水化物的酸性:HXO3>H3WO4 | |
| D. | 元素Z、W的最高正价分别与其主族序数相等 |
10.在下列有关装置中进行的实验,能达到目的是( )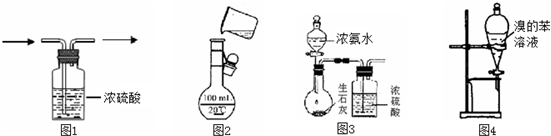

| A. | 图1用于除氯气中的水蒸气 | B. | 图2进行溶液的定容 | ||
| C. | 图3用于制取干燥的氨气 | D. | 图4用于溴与苯的分离 |
7.下列离子方程式书写正确的是( )
| A. | 将H2O2滴入酸性KMnO4溶液中:2MnO4-+10H++3H2O2=2Mn2++3O2↑+8H2O | |
| B. | 碳酸氢铵溶液和足量氢氧化钠溶液混合并加热:NH4++OH-$\frac{\underline{\;加热\;}}{\;}$NH3↑+H2O | |
| C. | 用惰性电极电解氯化钠溶液:2 H++2Cl-$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ | |
| D. | 1mol•L-1的NaAlO2溶液和2.5 mol•L-1的盐酸等体积混合:2 AlO2-+5 H+=Al(OH)3↓+Al3++H2O |
14.下列有关物质分离或提纯的方法错误的选项是( )
| 选项 | 物质 | 杂质 | 主要操作方法 |
| A | 溴苯 | 苯 | 加入铁粉和溴,过滤 |
| B | 氯化钠 | 氯化铵 | 加热 |
| C | 正丁醇,沸点117.7℃ | 乙醚,沸点34.5℃ | 蒸馏 |
| D | 乙酸乙酯 | 乙酸 | 加入饱和碳酸钠溶液,分液 |
| A. | A | B. | B | C. | C | D. | D |
1.化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用,如果设法提高化学反应的限度,下面说法错误的是( )
| A. | 能够节约原料和能源 | B. | 能提高产品的产量 | ||
| C. | 能够提高化学反应速率 | D. | 能够提高经济效益 |
8.在同温同压下,下列各组热化学方程式中,△H1>△H2的是( )
| A. | 2H2(g)+O2(g)═2H2O(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H1$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H2 |
5.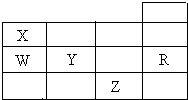 如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )
如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )
 如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )
如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )| A. | XZ3是平面正三角形分子 | |
| B. | 钠与X形成的化合物Na3X和NaX3都是含有共价键的离子晶体 | |
| C. | W与Y元素的最高价氧化物对应的水化物酸性前者弱于后者 | |
| D. | X的氢化物比W的氢化物稳定,但沸点前者比后者低 |
 +CO$→_{△}^{AlCl_{3},HCl}$
+CO$→_{△}^{AlCl_{3},HCl}$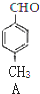 $→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$
$→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$ $→_{浓硫酸△}^{CH_{3}OH}$E
$→_{浓硫酸△}^{CH_{3}OH}$E .
.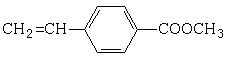 B.
B.
 D
D
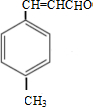
 .
.