题目内容
【题目】下列反应中,氯元素全部被氧化的是( )
A. 2P+3Cl2![]() 2PCl3
2PCl3
B. 2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
C. NaOH+HClNaCl+H2O
D. 2Cl2+2Ca(OH)2CaCl2+Ca(ClO)2+2H2O
【答案】B
【解析】
反应中氯元素全部被氧化,说明氯元素全部失电子化合价升高,发生氧化反应,据此分析解答。
A.该反应中Cl元素化合价由0价变为-1价,所以氯元素得电子化合价降低,全部被还原,A错误;
B.该反应中Cl元素化合价由-1价变为0价,所以Cl元素失电子化合价升高,全部被氧化,B正确;
C.该反应中没有电子转移,所以不是氧化还原反应,属于复分解反应,C错误;
D.该反应中Cl元素化合价由0价变为-1价、+1价,所以Cl元素被氧化、被还原,D错误;
答案选B。

练习册系列答案
相关题目
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g),体系中n(NO2)随时间的变化如表:
2NO2(g),体系中n(NO2)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)(mol) | 0.00 | 0.010 | 0.012 | 0.013 | 0.013 | 0.013 |
(1)写出该反应的平衡常数表达式:K=____________。已知:K(350℃)300℃),则该反应是________(填吸或放)热反应。
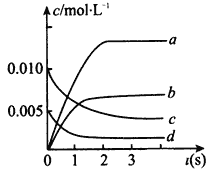
(2)下图中表示NO的变化的曲线是_________(填字母)用O2表示从0~2 s内该反应的平均速率v=_________。
(3)能说明该反应已达到平衡状态的是______________(填字母)
A.c(NO2)=2c(O2) B.容器内压强保持不变
C.v逆 (NO)=2v正(O2) D.容器内密度保持不变