题目内容
5.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )| A. | 45g水中含有的水分子数是2.5NA | |
| B. | 标准状况下,33.6LCO中含有的原子数是3NA | |
| C. | 0.5L、0.2mol/L的NaCl溶液中含有的Na+数是0.1NA | |
| D. | 1molCH4含电子数目为8NA |
分析 A.根据水的质量、摩尔质量计算出水的物质的量及分子数;
B.根据标况下气体体积及标况下的气体摩尔体积计算出一氧化碳的物质的量及含有的原子数;
C.根据n=cV计算出溶液中溶质氯化钠的物质的量,再计算出钠离子的物质的量;
D.甲烷含有10个电子,1mol甲烷含有10mol电子.
解答 解:A.45g水的物质的量为:$\frac{45g}{18g/mol}$=2.5mol,含有的水分子数是2.5NA,故A正确;
B.标况下,33.6L一氧化碳的物质的量为1.5mol,含有3mol原子,含有的原子数是3NA,故B正确;
C.0.5L 0.2mol/L的NaCl(aq)中含有溶质氯化钠0.1mol,0.1mol氯化钠中含有0.1mol钠离子,含有的Na+数是0.1NA,故C正确;
D.1molCH4中含有10mol电子,含电子数目为10NA,故D错误;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
13.已知Mg(OH)2的溶解度大于Fe(OH)3的溶解度.要除去混在MgCl2溶液中的FeCl3,可以边搅拌边加入一种试剂,这种试剂是( )
| A. | Na2CO3 | B. | NaOH | C. | Mg(OH)2 | D. | NH3•H2O |
20.不溶于水且比水轻的一组液体是( )
| A. | 甲苯、四氯化碳 | B. | 苯、汽油 | C. | 硝基苯、一氯丙烷 | D. | 酒精、溴 |
10.下列在给定状态下能导电的是( )
| A. | 固体氯化钠 | B. | 液态氯化氢 | C. | 乙醇溶液 | D. | 液态氢氧化钾 |
17.下列说法正确的是( )
| A. | 灼烧某白色粉末,火焰呈黄色,证明原粉末中含有Na+,无K+ | |
| B. | 实验中要配制500mL0.2mol•L-1KCl溶液,需用托盘天平称量7.45gKCl固体 | |
| C. | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,证明NH4Cl固体易升华 | |
| D. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加沸石 |
14.属于氧化还原反应的离子方程式的是( )
| A. | CaCO3+2H+=Ca2++CO2↑+H2O | B. | 2Fe2++Cl2=2Fe3++2Cl- | ||
| C. | HCO3-+H+=CO2↑+H2O | D. | H++OH-=H2O |
15.氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应中属于区域3的是( )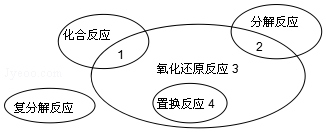

| A. | 2K2O2+2CO2═2K2CO3+O2 | B. | Cl2+2KBr═Br2+2KCl | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2NaHCO3═Na2CO3+H2O+CO2↑ |
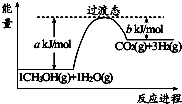
 2NH3(g)△H=-92kJ•mol-1.
2NH3(g)△H=-92kJ•mol-1.